Las terapias CAR-T han supuesto un cambio de paradigma en el tratamiento de algunas enfermedades oncohematológicas. En esta sesión de preguntas y respuestas, el hematólogo Víctor Noriega explica de forma muy práctica qué es la terapia CAR-T, en qué casos se indica, cómo es el proceso paso a paso y qué efectos secundarios deben conocer pacientes y familiares.
Si estás siguiendo contenidos de hematología en Espacio Pacientes, este artículo te interesará especialmente porque conecta con otros procedimientos habituales del día a día. Por ejemplo, puede ayudarte a entender mejor por qué, tras algunos tratamientos, se plantea un autotrasplante de médula o por qué en enfermedades como la leucemia linfocítica crónica (LLC) muchas veces se hace seguimiento sin tratar al inicio.
¿Qué es la terapia CAR-T?
La terapia CAR-T es un tipo de inmunoterapia: utiliza el propio sistema inmunitario para atacar células tumorales. No es “un único medicamento” válido para todo, sino una plataforma con la que se fabrican tratamientos personalizados según el tipo de enfermedad.
De forma sencilla: se toman linfocitos T (un tipo de glóbulo blanco) y se modifican genéticamente para que expresen en su superficie un receptor (CAR) capaz de reconocer una diana concreta en la célula tumoral. Así, cuando esos linfocitos CAR-T se reinfunden, pueden identificar y destruir células malignas que presenten esa diana.
¿Por qué no hay CAR-T para todo?
Para que un CAR-T sea seguro, la diana que reconoce (por ejemplo, CD19, CD20 o BCMA) debe estar presente en la célula tumoral y no en tejidos esenciales del organismo. Si esa misma proteína estuviese también en órganos como hígado, pulmón o intestino, los CAR-T podrían atacarlos. Por eso, desarrollar CAR-T para muchos tumores sólidos es más complejo: encontrar una diana “exclusiva” es difícil.
¿En qué enfermedades se usa?
En hematología, la plataforma CAR-T se ha desarrollado especialmente para atacar células malignas en:
- Linfomas (por ejemplo, algunos linfomas B con dianas como CD19).
- Leucemias (en escenarios concretos, según criterios clínicos y de financiación).
- Mieloma múltiple (con dianas como BCMA, en líneas específicas).
Un punto importante: cada CAR-T es “diana-específico”. Por eso se habla de CAR-T anti-CD19, anti-CD20, anti-BCMA, etc. No todos los CAR-T son iguales y tampoco tienen exactamente el mismo perfil de efectos secundarios.
¿Cuándo se considera candidato un paciente?
Esta es una de las dudas más habituales: “Si es tan innovador, ¿por qué no me lo pusieron de primeras?”. En la práctica clínica actual, el acceso depende de dos grandes bloques:
1) Criterios de indicación (líneas previas y situación de la enfermedad)
La terapia CAR-T suele utilizarse cuando se cumplen criterios establecidos (por ejemplo, tras recaídas o tras haber recibido determinadas líneas de tratamiento). En algunos casos, se está investigando su uso más precoz mediante ensayos clínicos, pero la realidad es que hoy suele reservarse para escenarios definidos.
2) Criterios de estado general (que el paciente pueda tolerarlo)
No basta con “cumplir criterios en el papel”. El equipo debe confirmar que el paciente está en condiciones de recibir el tratamiento: función cardiaca, pulmonar, renal, situación clínica general y capacidad para tolerar posibles complicaciones. Esto es clave porque los CAR-T pueden desencadenar una inflamación intensa en el organismo y, en casos graves, requerir soporte en UCI.
CAR-T vs trasplante de médula ósea: diferencias clave
Es frecuente comparar CAR-T con el trasplante porque ambos se usan en oncohematología, pero son estrategias distintas:
Trasplante autólogo
El autotrasplante se apoya en quimioterapia a altas dosis y en reinfundir células del propio paciente para recuperar la médula. No “dirige” el sistema inmune contra una diana concreta: su papel principal es permitir esa quimioterapia intensiva con rescate hematopoyético.
Trasplante alogénico
En el trasplante alogénico se infunde un sistema inmune nuevo procedente de un donante. Puede ayudar a controlar la enfermedad mediante un efecto inmunológico, pero también puede provocar complicaciones como la enfermedad injerto contra huésped.
CAR-T
CAR-T utiliza linfocitos (habitualmente del propio paciente) modificados para atacar de forma específica una proteína concreta. Es una inmunoterapia dirigida “proteína a proteína”, no un reemplazo completo del sistema inmune.
Fases del proceso CAR-T: qué esperar paso a paso
Una vez confirmado que el paciente es candidato, el proceso incluye varias fases. Entenderlas ayuda mucho a familias y pacientes porque hay tiempos de espera y decisiones clínicas importantes en el camino.
1) Evaluación y preparación
Se revisa el estado general y se completan pruebas (por ejemplo, cardiología o neumología si hace falta) para asegurar que el paciente puede tolerar el tratamiento.
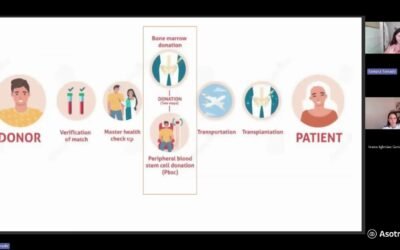
2) Leucoaféresis (recogida de linfocitos)
Se realiza una linfoaféresis para recoger linfocitos del paciente. Es un procedimiento similar a otras aféresis: se conecta al paciente a una máquina que separa y recoge los linfocitos, devolviendo el resto de componentes sanguíneos.
3) Fabricación del CAR-T
Los linfocitos se envían a una planta de fabricación donde se modifican genéticamente, se expanden y se preparan bajo estrictos controles de trazabilidad y calidad. El producto final llega al hospital normalmente congelado, en un volumen pequeño (una “bolsita” con el medicamento celular).
El tiempo de fabricación puede variar. Por eso, mientras se espera, el equipo debe decidir si la enfermedad permite aguardar o si necesita tratamiento para controlar la situación.
4) Tratamiento “puente” (si es necesario)
Durante la espera, algunos pacientes necesitan una terapia puente para controlar la enfermedad. El objetivo es ganar tiempo sin permitir que la enfermedad progrese de forma peligrosa.
5) Quimioterapia de linfodepleción (antes de la infusión)
Antes de infundir los CAR-T se administra una quimioterapia corta (habitualmente durante 3 días) llamada linfodepleción. Su función es “hacer espacio” reduciendo linfocitos previos para facilitar que los CAR-T se expandan y funcionen mejor.
6) Infusión del CAR-T
La infusión se realiza por vía venosa, de forma similar a una transfusión, utilizando un acceso venoso adecuado. A partir de aquí, el equipo monitoriza de cerca los primeros días, que es cuando suelen aparecer los efectos secundarios más relevantes.
Efectos secundarios principales: lo que más preocupa (y por qué)
Los dos efectos más llamativos suelen aparecer en los primeros días tras la infusión, aunque el momento exacto depende del tipo de CAR-T, de la enfermedad y de la carga tumoral.
1) Síndrome de liberación de citocinas
Es una reacción inflamatoria causada por la activación de los linfocitos CAR-T al reconocer la enfermedad. Puede manifestarse con fiebre, cansancio intenso, dificultad respiratoria, necesidad de oxígeno, retención de líquidos e inestabilidad clínica. Hay formas leves que se controlan en planta y formas más graves que pueden requerir UCI.
2) Neurotoxicidad
Puede aparecer después del síndrome inflamatorio o de forma aislada. Los síntomas varían: dolor de cabeza, desorientación, dificultad para hablar, cambios de conducta o, en casos poco frecuentes, alteraciones graves del nivel de consciencia. La buena noticia es que, con experiencia y vigilancia, identificar precozmente los síntomas permite actuar antes de que el cuadro progrese.
3) Citopenias e infecciones (más tardías)
Tras la fase aguda, algunos pacientes presentan bajada de defensas, anemia o plaquetas bajas, lo que aumenta el riesgo de infecciones y puede requerir seguimiento estrecho e incluso transfusiones en las semanas posteriores. En algunos casos se pautan medidas de prevención (profilaxis antibiótica/antiviral) y, si hay descenso de inmunoglobulinas, puede valorarse administrar inmunoglobulinas periódicamente.
Señales de alarma tras el alta: cuándo consultar sin esperar
Cuando el paciente se va a casa, se recomienda estar acompañado y vigilar signos que, aunque a veces sean leves, conviene revisar cuanto antes:
- Fiebre o sensación de empeoramiento general.
- Desorientación, conducta extraña, dificultad para hablar o somnolencia llamativa.
- Dificultad para respirar, sensación de falta de aire o empeoramiento progresivo.
- Infecciones o síntomas persistentes que no ceden.
Ante duda razonable, lo prudente es consultar. En estos tratamientos, actuar temprano marca la diferencia.
Preguntas frecuentes que ayudan a aterrizar expectativas
¿CAR-T “cura” siempre?
Es una terapia muy potente y ha mejorado resultados en pacientes con opciones limitadas, pero no funciona igual en todos. En algunos casos se logran respuestas duraderas, y en otros la enfermedad puede reaparecer. Por eso el seguimiento y la selección del paciente son fundamentales.
¿Se usará cada vez antes?
Se investiga su uso en líneas más precoces para pacientes con características de alto riesgo. La tendencia general en medicina es personalizar: usar CAR-T antes en quienes más se benefician y reservar otras estrategias para quienes tienen buen pronóstico con tratamientos estándar.
¿Existen CAR-T “de donante” listos para usar?
Se están estudiando CAR-T alogénicos (de donante) para reducir tiempos, pero aún es un campo en desarrollo. Si en el futuro se consolidan, podrían acortar esperas y simplificar logística.
Idea clave para llevarse
Las terapias CAR-T son una inmunoterapia avanzada y personalizada que utiliza linfocitos T modificados para atacar dianas específicas del tumor. El proceso incluye recogida de células, fabricación, posible terapia puente, quimioterapia corta previa e infusión, con vigilancia estrecha por riesgos inflamatorios y neurológicos. Con buena selección y control clínico, se ha convertido en una opción transformadora para muchos pacientes.
Para ampliar: si quieres entender mejor cómo encajan las distintas estrategias en oncohematología, te recomendamos leer también Autotrasplante de médula: qué es y para qué sirve y este resumen de Leucemia linfocítica crónica (LLC), donde se explica por qué en algunas enfermedades se prioriza el seguimiento y en otras se requieren terapias dirigidas.
Ver transcripción del vídeo
00:00:07 Buenas tardes. Eh, hoy vamos a abordar eh un tema esencial como son las terapias CARTI. En los últimos años, la terapia CARTI ha supuesto un cambio de paradigma en el abordaje de determinadas enfermedades oncomatológicas, abriendo nuevas posibilidades terapéuticas para pacientes que previamente contaban con opciones limitadas. Así que hoy contamos con el hematólogo Víctor Noriega para profundizar qué es esto de la terapia CART, en qué casos está indicada y qué implica realmente este tratamiento en en la práctica clínica. Así que nada, si te
parece te iré preguntando cuestiones básicas, perdón, que cualquier paciente o familiar pues debería conocer sobre sobre esta terapia. Así que nada, primera pregunta y más básica, ¿no?, que es esta terapia CARTI y cómo se reeducan, ¿no?, estas células del paciente para tratar un cáncer hematológico. Eh, bueno, primero muchas gracias por invitarme a participar. encantado de intentar resolver, bueno, pues todas estas dudas acerca de esta de esta nueva terapia que ha creado tanta expectativa, ¿no? Pero bueno, hay que poner un un
poco de realidad y yo creo que es eh muy bueno para los pacientes, familiares, eh etcétera. Lo primero que hay que saber es que la terapia CART es una es una terapia es un tipo de inmunoterapia y es una plataforma, por decir así, yo siempre lo intento explicar así a los pacientes en que es una plataforma para fabricar un tipo de medicamento, ¿no? Es decir, no hay un carté que valga para todos los pacientes ni para todas las enfermedades, sino que la terapia carté utiliza una plataforma en la que se diseñan y se fabrican medicamentos que
luego, como veremos a lo largo de la de la charla, pues están eh ideados para un determinado tipo de enfermedad, ¿vale? O sea, que cuando decimos Karté, hablamos de una plataforma de tratamiento, un tipo específico de tratamiento que se basa en la inmunoterapia, en utilizar el sistema inmune para atacar, en este caso, en las en el caso de las enfermedades hematológicas, a las células, por decir así, malignas, ¿no?, al tumor hematológico, ¿vale? Pero en otros casos esta plataforma se podría utilizar para atacar a otro tipo de
células, ¿vale? Eso es un poco el el concepto, ¿vale? En el caso de hematología, eh, lo que y en el caso de los de los carté, lo que viene definido es por eh utilizar el sistema inmune para atacar a las células malignas hematológicas, ¿vale? En el caso de un mieloma a las células del mieloma, en el caso de un linfoma a las células del linfoma y en el caso de una leucemia a las células de la leucemia. ¿De acuerdo? Vale, utiliza eh son como eh utiliza el aprendizaje que los hematólogos hemos tenido a lo largo durante de muchos años
eh de dos estrategias de tratamiento. Por un lado, los anticuerpos monoclonales, que son unas proteínas que somos capaces de diseñar para que ataquen, se unan a una proteína específica de las células y la ataquen. ¿Vale? Nosotros ya lo sabemos y seguramente los pacientes pues conocerán en el caso del linfoma, por ejemplo, el rituximap que es una proteína que ataca al CD20, ¿vale? Es una proteína específica y está diseñada para que ataque a esa célula y la destruya, ¿vale? Pues tenemos por un lado ese anticuerpo monoclonal y luego por otro
lado tenemos eh los linfocitos. Los linfocitos son un tipo dentro de los glóbulos blancos de que todos los los todas las personas tenemos existen diferentes tipos de de glóbulos blancos. están los neutrófilos, los macrófagos, eh los linfocitos B, los células NK y luego hay unos que un subtipo que son los linfocitos T, ¿vale? Entonces, los linfocitos Tenerísticas eh muy específicas y en condiciones normales lo que hacen es que pues viajan por nuestro organismo y nos ayudan a luchar contra infecciones, a reconocer
las eh las células propias o las células eh eh no propias o ajenas. nos ayuda a luchar contra bacterias, contra virus, etcétera, pero también tiene una una capacidad de que por sí mismos y en condiciones normales son capaces de identificar incluso a eh células tumorales que son como anormales dentro de nuestro cuerpo, ¿no? Entonces, nosotros ya sabemos por la nuestra historia del uso de los glóbulos blancos para tratar a enfermedades. En este caso, lo que hacemos en el trasplante de médula ósea, cuando utilizamos un
donante distinto del receptor, lo que queremos es que esos linfocitos ataquen al tumor, ¿no? Pues en este caso, conociendo eso, ¿no? Sabemos que los linfocitos T son capaces de de alguna forma eh ese sistema inmune hacer que ataque al tumor. ¿Vale? Entonces, tenemos por un lado este anticuerpo monoclonal y por este otro lado los linfocitos T. ¿De acuerdo? Pues la terapia carte lo que hace es que modifica de manera genética estos linfocitos T, ¿vale? Para que sean capaces de de expresar en su superficie el anticuerpo monoclonal que nosotros
hemos diseñado. ¿De acuerdo? De forma que cuando nosotros eh introducimos estos linfocitos T, ya que son CART, por eso se llama células T, eh kimeric antigenon receptor T cell, ¿de acuerdo? Son células T cargadas con un receptor quimérico antigénico. Esto es un poco más complejo, pero para que nos hagamos una idea es este anticuerpo monoclonal, las células T, que en condiciones normales no lo tienen, son capaces de expresarlo en su superficie. De forma que cuando nosotros introducimos estas células en un paciente, estos linfocitos
T que en condiciones normales harían su trabajo, además de hacer su trabajo, son capaces de manera específica reconocer eh eh la proteína para la cual tiene en su superficie esta molécula, ¿vale? Entonces, si nosotros tenemos KT y le ponemos esta molécula en la superficie que es anti20, ¿vale? Pues tenemos un CT anti de 20. Si le ponemos anti19, tenemos un carté anti19. Si le ponemos que vaya contra una molécula, en el caso del mieloma que se llama BCMA, tenemos un carté anti BCMA, ¿vale? De ahí un poco la peculiaridad. Entonces, esto es
un poco eh a grandes rasgos lo que es un un un KT, una célula Karté, cómo se cómo se construye, ¿no? Si vas a hacer como en medida, ¿no? Un poco muy específico, muy Exacto. Exacto. Porque son eh son tratamientos que están eh diseñados específicamente para atacar un tipo de célula, ¿no? Así como con la quimioterapia, en condiciones normales, tú le pones un paciente una quimioterapia y puede ser más o menos efectiva contra un tipo de células, siempre provoca daños, ¿no? En otras células que en realidad a lo mejor tú no
querrías. En este caso, si tú le pones una terapia carté, en este caso, por ejemplo, anti19 a un paciente, esas células, esos linfocitos, van a ir por el organismo y van a atacar a todos los sitios donde encuentren CD19, ¿vale? En este caso es en la médula ósea o en la sangre, ¿vale? En los ganglios, eh, y no lo hay en ningún otro sitio. Por eso no hay muchos carté contra muchas enfermedades, porque identificar una proteína que esté solo en el tumor, pero que no esté en otros sitios es muy complicado, porque si no tú le pondrías
un carté contra una célula tumoral, pero a lo mejor una célula del hígado o una célula del páncreas o del intestino o de los pulmones que es normal, puede tener esa proteína. y estos cartés no lo van a diferenciar, ¿vale? Por eso no hay cartés contra muchos tipos de tumores, ¿no? Entonces, en el caso de los linfomas, afortunadamente es muy específico y esa proteína no está en otros tejidos del cuerpo. Vale, vale, vale. Bueno, otra pregunta que yo se la escucho a, bueno, a muchos pacientes, ¿no? Que al final pues fuera
un autotransplante hubo una recaída, fuera una transplante de progenitores hematopoyéticos, hubo una recaída y finalmente dicen, «Vale, pues eres candidato a un cantí, ¿no?» Entonces, e es un poco en qué momento del proceso oncoatológico se considera que el paciente es candidato a un cartí, ¿no? Porque muchos dicen, claro, si este fue el tratamiento definitivo y es algo como tan innovador, ¿por qué no me lo pusieron de primeros? ¿Qué criterios existen para que yo pueda acceder o o no pueda acceder? Vale. Eh, ahora mismo, en
la actualidad, a día de hoy, eh, diciembre de 2025, que es cuando estamos teniendo esta conversación, actualmente existen eh terapias carte, medicamentos financiados por el sistema nacional de salud, ¿de acuerdo? Eh, en mieloma, ¿vale? En mieloma en paciente es que tienen que cumplir eh, no es que no se le puedan administrar, es que están financiados en una situación muy concreta de la enfermedad. Entonces, en el caso del mieloma ahora mismo está aprobado para pacientes que eh han completado o que o que han han recibido
una línea de tratamiento con una serie de fármacos y que además ha sido refractario a uno de ellos, ¿vale? Si no cumple esos requisitos, el CAR no se le puede administrar, ¿vale? Esto en cuanto a la enfermedad. En el caso de los linfomas, eh se está aprobado en pacientes con linfoma difuso de célula grande B que han recaído a una primera línea de tratamiento, pero que por que esa recaída ha sido precoz en los primeros 12 meses, ¿vale? Si no es así, eh hay que desgraciadamente no hay capacidad de poner un carte hasta que el
paciente haya recibido al menos dos líneas de tratamiento y haya recaído posteriormente. ¿Vale? En el caso de la leucemia aguda linfoblástica, pues ocurre una cosa parecida. tiene que haber recaído previamente. En el caso del linfoma follicular, también del linfoma del manto. Es decir, el hm el paciente tiene que cumplir unos requisitos que están establecidos por lo que es la financiación que el ministerio ha aprobado. ¿Vale? Lo que eh ha ocurrido y lo que ocurre con generalmente con los fármacos que funcionan bien es que al principio se
utilizan en situaciones, vamos a decir, no desesperadas, pero complicadas. Es decir, en aquella situación en la que los pacientes ya han han fracasado muchos tratamientos. Entonces ahí, bueno, pues hay un porcentaje de pacientes que responde bien, pero desgraciadamente muchos no. Lo que se ha visto concarté en determinadas circunstancias, en otras todavía no está muy claro, es que si nosotros eh utilizamos los cartés en situaciones más precoces, es decir, no esperar a que el paciente haya agotado ya muchos tratamientos, imagínate en mi cinco
tratamientos vamos a ponerle un cartel, ¿no? Lo que se ha visto es que si se lo pones antes en a lo mejor después de haber recaído solamente una vez, pues los resultados a largo plazo son mucho mejores. ¿Vale? Eso es lo que está ocurriendo. Eso es lo que está ocurriendo. Incluso ahora mismo hay ensayos clínicos que ya están intentando utilizar la terapia Carté desde en la primera línea de tratamiento, ¿vale? Habrá que ver qué resultados tienen y habrá ver que determinados pacientes se benefician de eso y ahora
hay algunos pacientes que se benefician de seguir el tratamiento estándar, ¿no? Eso es un poco la situación. Ahora hay una cosa importante de decir es eh cuando un paciente dice si se es o no candidato, hay dos cosas importantes ahí, porque una cosa es que el paciente cumpla los criterios, por decir así, de la ficha técnica, ¿no? En el papel, yo tengo un un un paciente con un linfoma que ha recaído después de dos líneas, tal, cumple los criterios para este. Bien, pero luego hay que ver que el paciente está en condiciones de recibir
ese tratamiento, ¿vale? Que son cosas muy distintas. Y cuando hablamos de que está en condiciones es que orgánicamente tiene que tener bien su función pulmonar, su función cuarríaca. El riñón tiene que funcionar bien, es decir, tiene que cumplir unos requisitos físicos, ¿vale?, que eh hagan que se le pueda administrar ese tratamiento. Y esto es muy importante porque eh la terapia cart que decimos, «Bueno, pues me ponen este tratamiento y ya está, estos linfocitos y así eh vuelvo un poco para atrás, pero lo dejé a drede para
explicarlo ahora. Eh, estos linfocitos T, estos CT, cuando nosotros los infundimos al paciente y empiezan a funcionar, ¿vale?, se se activan y es un es un medicamento vivo, ¿no? Entonces, son células vivas que lo que hacen por el organismo es lo que les toca hacer de linfocitos. Entonces, cuando reconocen esas células contra las que han sido diseñadas, pues se activan y al activarse, pues empiezan a segregar una serie de eh proteínas, etcétera, que van a destruir la célula, pero que a la vez van a crear una inflamación en todo el
organismo. ¿Vale? Entonces, o sea, hay que hay que saber que el cuerpo puede aguantar, ¿no?, también todo el proceso. Efectivamente, efectivamente. Y esa inflamación, que es un lo que es una de las principales complicaciones, eh se llama un síndrome de liberación de citocinas, ¿vale? Y eso puede ser desde una cosa muy leve hasta que el paciente tenga que irse a la UCI porque no es capaz de respirar, ¿vale? Además de eso, también hay una toxicidad, un efecto secundario consecuencia de toda esta inflamación que es a nivel neurológico y
que puede ser también muy grave, ¿no? Entonces, como sabemos que tienen estas complicaciones, cuando nosotros eh hablamos de que un paciente es candidato, además de que por un lado la enfermedad cumpla los requisitos, tenemos que estar seguros de que el paciente físicamente está en condiciones de recibirlo y de que si ocurre alguna de estas complicaciones va a poder sobrellevarlas, ¿vale? Vale, vale. ¿Y crees que en el futuro ese KTI empezará a aplicarse como antes de Porque ahora un poco hablamos de líneas de tratamiento fallidas, ¿no?
Entonces, ¿cómo prees que podría en una hipótesis? ¿No? Hay hay una una cosa importante que eh muchas veces y que esto suena así un poco eh bueno, pero yo siempre lo cuento porque creo que además el paciente muchas veces eh quiere oír esa sinceridad, ¿no? Y es decir, estos son tratamientos que están mejorando eh los resultados de otros tratamientos, ¿vale? Pero que desgraciadamente no funcionan bien en todos los pacientes, ¿vale? Eso es una cosa que que es decir, no decir, bueno, me van a poner esto y con esto ya, bueno, pues
desgraciadamente nos gustaría que sí, pero todavía no. Lo que se ve es que en determinados pacientes y en determinadas circunstancias si adelantamos, es decir, no esperamos a ponerle ese tratamiento a que el paciente haya recaído una o dos veces, ¿vale?, pues los resultados son mejores, ¿vale? Pero sin embargo, a lo mejor hay pacientes que con los tratamientos que tenemos o con otros el resultado va a ser el mismo, ¿vale? O sea, que eso todavía no está muy claro. Lo que sí que es verdad es que en determinados pacientes, a lo mejor
pacientes que por las características que tienen cuando se diagnostican o por cómo han evolucionado durante el primer tratamiento, hay algunos pacientes que a lo mejor se benefician de ser, por decir así, más agresivo utilizando este tipo de terapias al principio y no esperar a que el paciente recaiga. ¿Vale? Eso sí que es un poco hacia donde se está viendo, no ponérselo a todos los pacientes, sino ponérselo a los pacientes que lo necesitan o que que más se van a beneficiar de él, ¿no? Y si eso significa ponérselo al principio, pues
significará ponérselo al principio. Si eso significa, pues un paciente que a lo mejor tiene unas características de muy buen pronóstico, pues a lo mejor no tienes que ponerle esto al principio, sino que si tú sabes que va a estar muchos años libre de enfermedad y muy bien, pues no tienes por qué gastar esta tratamiento. Al principio a lo mejor se lo puedes dejar para posteriormente. Vale, vale. Y otra pregunta, ¿qué diferencia hay realmente entre un cartí y el trasplante de médula ósea? Eh, haí grande, ¿vale? en en los trasplantes. Sé que hay
creo que hay alguna charla, alguna alguna reunión vuestra que hablaréis de lo que es el trasplante autólogo, trasplante halogénico, etcétera. Eh, un poco eh en cuanto al trasplante autólogo, que el trasplante autólogo no deja de ser más que una quimioterapia a altas dosis. Un poco la plataforma es más o menos la misma de lo que es eh lo que hay que hacer con el paciente, ponerle primero quimioterapia, etcétera. Eh, hablaremos luego de esto de cómo cómo son todos los pasos. Eh, y lo que se utilizan son células del propio
paciente, ¿vale? De acuerdo. Eh, que es lo que utilizan, lo que esas células lo único que hacen es pues bueno, regenerar la médula para que poder ponerle una quimioterapia fuerte. En el caso del trasplante halogénico, que es un poco probablemente eh hmoterapia que el trasplante autólogo, en el trasplante alogénico nosotros al paciente le ponemos un sistema inmune nuevo, completo, y ese sistema inmune hace su labor de sistema inmune y entonces eh intenta eh pues hace fabricar glóbulos blancos, linfocitos T, linfocitos B, etcétera, etc. Pero
también puede provocar efectos secundarios en todo el organismo porque va por el organismo y va diciendo, «Uy, este no es mi hígado, este no es mi esta no es mi piel.» y puede provocar esta enfermedad que conocemos como la enfermedad de injerto contra huésped, pero a su vez también este sistema inmune va a proteger al paciente para que la enfermedad no recaiga, porque si aparecen células otra vez malas, las se supone o la que queremos es que este sistema inmune nuevo lo ataque, ¿no? Pero lo ataca de una forma general, ¿no?
No lo ataca de una forma general. Entonces, el el el es el propio sistema inmune global el que ataca a la enfermedad. En el caso de la terapia CART son linfocitos que han sido diseñados específicamente para atacar a una célula que tiene en la superficie de la célula una proteína. Es decir, es proteína a proteína, no es el sistema inmune completo, no es una terapia dirigida que decimos el el eh le le le damos un sistema inmune, pero dirigido contra una cosa, mientras que en el trasplante halogénico al paciente
le infundimos un sistema inmune nuevo completo, por decir así. ¿Vale? Esto me lleva también a decir que cuando hablamos ahora o lo que está comercializado y que utilizamos ahora como terapia carté en esto utilizamos células del propio paciente, lo que está comercializado ahora mismo, ¿vale? Pero eh hay ensayos y hay estudios que están trabajando en utilizar eh células de un donante como fuente para fabricar el cartel, ¿de acuerdo? Es decir, en vez de utilizar mis propios linfocitos, sino utilizo los de otro, los de los de un
donante. ¿De acuerdo? Y eso uno dice, «Bueno, pero entonces, digo, no, eso qué ventaja tendría.» Pues luego veremos cuáles son los pasos de fabricar un un este tipo de de terapias que llevan eh una logística, etcétera, y si tú eres capaz de tenerlos en una nevera congelados ya previamente, pues pasaría a ser un medicamento más que está en la farmacia con una ventaja. Tiene sus inconvenientes, ¿vale? y parece que está costando más llegar al a a lo que es el bueno, los ensayos les está costando un poquito más, pero también es una es una
idea de futuro que probablemente esté ahí, ¿no? utilizar los card alogénicos, es decir, de un donante, de forma que estén ya fabricados y guardados en una repisa en la farmacia para cuando los necesites utilizar, porque como veremos luego que hablaremos de las fases de cómo se se fabrica un card y todos los tiempos que lleva, veremos que hay sería una gran ventaja. Vale. Vale. Veo que es como que todo cada vez va diseñado, cada vez va más específico a dónde tiene que ir, ¿no? que es como la gran línea que que se
pretende y y esa era la siguiente también pregunta, ¿no? Es cuáles son las fases es decir, vale, soy candidato a a ese cartí y desde esa extracción de de linfocitos, ¿qué fases cabe esperar? ¿Qué va a pasar ahí, no? Una vez que estoy dentro, por así decirlo. Vale, lo primero es eh lo que estábamos hablando antes de la la selección del candidato, ¿vale? Hay una aquí lo que ocurre desgraciadamente es que estamos hablando a día de hoy en la situación en la que estamos, el glosscart siempre se están utilizando en pacientes que ya han
recibido un tratamiento para su enfermedad y que desgraciadamente la enfermedad no va bien, ¿vale? Con lo cual eh todo lo que voy a contar ahora eh va a ser todo con el paciente teniendo su enfermedad, en cierto modo con mayor o menor urgencia en recibir un tratamiento, ¿vale? Porque sabemos que hay veces que la enfermedad aparece, pero el paciente se encuentra bien y tenemos tiempo para hacer determinadas cosas, estudios, etcétera, pero hay veces que hay enfermedades que son muy rápidas, ¿no? Y que progresan, tienen muchos síntomas y
que no podemos esperar para poner tratamiento. ¿Vale? ¿A qué cuento? ¿Por qué cuento esto? Porque primero hay que estar seguros de que el paciente cumple todos los criterios y que además físicamente está bien. ¿De acuerdo? Entonces, por ejemplo, tenemos un paciente que ha tenido un infarto, que tiene problemas de corazón. Muchas veces para saber eso, pues a lo mejor necesitamos que antes de que poner en marcha todo, que le que le vea un cardiólogo, que le haga una prueba cardiológica, etcétera, para nosotros
estar seguros de que está en las condiciones óptimas para continuar, ¿vale? Entonces ahí ya tenemos, bueno, pues una serie de cosas que hay que hacer antes, ¿vale? como un checklist, ¿no? A modo hay que cumplir. Exacto. O el neumólogo o a lo mejor tiene un problema en el riñón. Hay cosas que se pueden decir, bueno, pues esto no efectivamente lo tiene, pero no es problema. Pero hay veces que sí. Bueno, ese tipo de cosas. Es decir, todo eso es como burocracia de papeleos, de cosas que hay que hacer antes de empezar con
todo este proceso, ¿vale? Eh nosotros generalmente eh todo esto lo hacemos en paralelo con poner en marcha las fechas de eh los determinados procesos que hay que hacer. Es decir, aunque el paciente esté pendiente de una consulta de cardiología, a lo mejor nosotros ya le tenemos una fecha de aféresis asumiendo que va a ir todo bien, ¿vale? Es decir, no esperamos a que se cumpla un paso para ir al siguiente porque si no nos eternizaríamos. Entonces, eh una vez que nosotros tenemos el paciente está OK, por decir así, ¿vale? Lo
primero que hay que hacer es una afresis, que es un procedimiento, una linfoféresis, que es recoger células en este caso, del propio paciente, ¿vale? eh que es un procedimiento muy parecido al de los trasplantes. Lo único que no necesitamos estimular la médula con las inyecciones de zarcio y ese tipo de cosas, sino que simplemente es un procedimiento de conectar al paciente y recoger. La máquina se puede diseñar para que haga diferentes cosas y en este caso se diseña para que recoja solo linfocitos. ¿Vale? ¿De acuerdo? Entonces, eso se
hace eh desde que se hace esa recogida de los linfocitos eh eh rebobino, recogemos los linfocitos y esos linfocitos nosotros los tenemos que enviar a una fábrica que es donde se va a fabricar el cart. Esto que decía yo antes de hacer que el linfocito sea capaz de producir en la superficie, pues eso se hace una fábrica. Eso es como una ingeniería, ¿no? Un poco es una ingeniería total, ingeniería genética total, ¿vale? Y eso se hace en una fábrica, en una serie de condiciones. Ahora, actualmente son eh una fábrica por una empresa comercial,
que son los que fabrican el medicamento, ¿vale? Entonces, desde que se hace recogen las células, se envía a la fábrica, lo fabrican y lo devuelven al hospital para poder ponérselo al paciente, ¿vale? Hay algún producto, alguno de los medicamentos que está durando en torno a 17 18 días, pero hay otros que duran cinco o se que tardan cinco o se semanas o cuatro o c semanas, ¿vale? Entonces, ¿por qué hablo de esto y hablo de estos tiempos? Porque lo que decía antes, si el paciente tiene una enfermedad que a lo mejor está un poco
tranquila y podemos esperar bien, pero si la enfermedad está ahí, eh, no podemos no hacer nada, ¿no? Entonces, hay que jugar con estos tiempos y con la enfermedad y con el paciente, ¿vale? para la toma de decisiones. Y muchas veces en este periodo entre que recogemos las células y recibimos las células a los pacientes hay que ponerles tratamiento para controlar la enfermedad, ¿vale? Incluso para disminuirla si es posible, ¿vale? Y es lo que nosotros llamamos la terapia puente. Terapia puente al CARP. Muy sencillo y muy y muy gráfico, ¿vale?
Y hay veces que hay pacientes que tienen que recibir una línea o incluso dos dos líneas de tratamiento en este periodo, ¿vale? Entonces, esta es la primera fase. Primero, identificar y okay, con el paciente, todo bien, hacemos todo el papeleo, el Ministerio de la prueba es aprobado, hacemos esta linfoféis, ¿de acuerdo? Y después de la linfoféis eh se estos linfocitos se mandan a fabricar a una fábrica. Por decir, si suena, no me voy a meter mucho más, pero es un poco más complejo, eh, todo lo que hacen la fábrica, eso nos lo devuelven y nos lo
devuelven en una bolsita congelada. específico para esa persona. Exacto. Eh, en este caso, en este tipo de card, por eso digo que si hubiese cart alogénico de un donante, podríamos tener ya esa bolsita ya fabricada en la nevera sin tener mucho tiempo. Exacto. Exacto. Entonces, eso es un es una ventaja muy importante, pero todavía le falta tiempo. también hay ensayos clínicos, etcétera, pero bueno, está costando más de lo que de de de lo de lo que se creía y bueno, está costando más trabajo, ¿de acuerdo? Perdón. Entonces,
eso nos lo devuelven en una bolsita y esa bolsita lo que trae son linfocitos del propio paciente, ¿vale? siguiendo un sistema de calidad eh y trazabilidad que asegura que no ha habido ningún problema, que siguen siendo sus linfocitos, que no se ha cruzado con nada, infecciones, todo ese tipo de cosas, está todo controladísimo. Y lo que nos devuelven es un producto, una cajita pequeñita que además lleva generalmente son mililitros, o sea, hablamos de 50, 60 ml o menos incluso. En función del CAR cambia, ¿vale? Hay
alguna variedad porque a veces son un tipo de célula y otro tipo de célula. Bueno, eso, pero en principio son viene congelado, ¿no? Y nosotros eso lo guardamos en la nevera, en un congelador específico, por decir así, hasta que el paciente está preparado para iniciar todo el proceso de que que veremos a continuación. Pero viene eso, una pequeña bolsita en la que es un producto en el que está lleno de células y que el 99 no sé cuánto por cento son linfocitos T K específicos para el el en este caso el linfoma, el mieloma y son los propios
linfocitos del paciente. ¿Vale? O sea, esas serían eh Vale. Y esa quimio, existe, o sea, hay una quimio previa, la quimio de barrido, llamamos a químio de barrido, ¿no? Eh, ¿cuándo se eh realiza? Porque tiene que calcularse los días justo antes de o hay un tenemos que jugar ahí con tiempos o no. No, eh hay una serie de tiempos muy específicos con los que hay que contar. Unos de ellos son eh básicamente antes de recoger las células, antes de la linfoféis, el paciente tiene que estar, si ha recibido un ciclo de
quimioterapia, tiene que estar 4 semanas sin recibir quimioterapia, ¿vale? Si es otro tipo de tratamiento, a lo mejor pues a ver, los pacientes de mieloma sabrán la lenalidomida, pomalidomida, etcétera, esos el margen de tiempo es menor, ¿de acuerdo? Con lo cual por eso digo que es muy importante los tiempos. Entonces, antes de la leucaféis, el paciente tiene que estar un tiempo sin tratamiento, ¿de acuerdo? Pero eh en cuanto a la vez que ya está todo preparado y el paciente ha recibido una quimioterapia, eso es un poco más eh
laxo, o sea, no no es tan riguroso en esta en esta segunda fase, ¿vale? Entonces, eh antes de poner el tratamiento, el cártel, porque tú podrías ponérselo a un paciente según llega, se lo pones y ya está. Pero lo que se ha visto es que los resultados son mucho mejores cuando al paciente se le pone eh unas pequeñas dosis de quimioterapia antes, unos días antes, ¿vale? Por eso lo de los cálculos de estos días. Y lo que se ha visto es que hay dos fármacos que son fluarabina y ciclofosfamida, que son los que mejor
resultado dan a porque son, por decir así, fármacos que actúan contra los linfocitos. Entonces estos tú se los pones al paciente durante 3 días. Una dosis de quimioterapia que desgraciadamente para lo que muchos pacientes reciben no es mucha cantidad y se tolera generalmente bien durante 3 días. Y esto lo que hace es que barre el barre al paciente es como que le quita todos los linfocitos. Los linfocitos, ¿vale? Y deja hueco para los linfocitos que nosotros le vamos a poner, ¿no? Y que le vamos a dar para que esos linfocitos crezcan y hagan lo
que tienen que hacer, ¿vale? Entonces es una quimioterapia que se llama quimioterapia de linfodeplexión, ¿vale? Vale. Y es específica para esto, ¿de acuerdo? es una quimioterapia que es una dosis pues normaliza, tampoco es muy exagerada, se pone durante 3 días, se deja descansar 2 días, aunque pueden ser más, no pasa nada, y luego se ponen eh se se infunden por por un catéter, por la avena, este medicamento carte, que son los linfocitos carte. Vale, vale. Bueno, y ya un poco también para finalizar y algo que preocupa
bastante a pacientes es eh bueno, efectos secundarios, ¿no? Al final es como antes hablaste del síndrome de liberación de citocinas y también de la neurotoxicidad y que hay diferentes grados, ¿no? Un grado a lo mejor leve se soluciona pues en planta con una medicación, pero un grado un grado más grave pues en UCI, ¿no? Entonces, ¿qué efectos secundarios que habría esperar? ¿No? Los los principales efectos secundarios son los los principales o los más llamativos, los más así potentes, por decir así, son estos dos, porque ocurren
eh generalmente al principio, en los primeros 10 días, 10, 14 días, muchas veces incluso antes, vamos a decir entre los en los primeros 7 días, 7 10 días, una cosa así, ¿vale? Y esto es muy variable. Es muy variable. Es muy variable porque depende de muchas cosas. Depende primero del tipo de card que estamos poniendo. Es distinto el síndrome de liberación de citocinas o la neurotoxicidad de un CART anti CD19 que un CART anti BCMA. Por eso quería dejar bien claro antes que los CART no son todos iguales, sino y que más cada uno
tiene sus peculiaridades, sus efectos secundarios más específicos, etcétera, ¿no? Entonces, eso es lo primero que hay que ver. Primero, ¿qué tipo de tratamiento le vas a poner al paciente? ¿No? Si tú ingresas a un paciente para un card de mieloma, pues esperas un tipo de complicaciones y en unas fechas. Si es un si luego también depende de eh el tipo de enfermedad, si es un linfoma, si es una leucemia, tal, de cómo esté decontrolada o no controlada la enfermedad. Desgraciadamente, cuando tú pones estos tratamientos, como son
células vivas, si al ingresar al al entrar en el cuerpo reconocen mucha enfermedad, ¿no? Y el cuerpo está muy inflamado, se inflaman mucho, entonces tienen más riesgo de desarrollar estas complicaciones, ¿vale? Esta inflamación tan gorda que es el síndrome de liberación de citocinas. Sin embargo, si la enfermedad está muy controlada y el paciente se encuentra muy bien, pues el riesgo de desarrollar esto a lo mejor es igual, pero no va a hacer eh grados eh severos de estas complicaciones, ¿vale? Entonces, hay una serie de cosas que tú
tienes que saber antes. Hay una serie de scores que nosotros sabemos un poco para calcular más o menos un poco a ojo el riesgo que tiene cada paciente al empezar de desarrollar estas complicaciones, ¿vale? Y básicamente son este síndrome de liberación de citocinas y la neurotoxicidad. El síndrome de liberación de citocinas es eh una inflamación muy fuerte en el organismo, ¿vale? Que básicamente es fiebre, eh dificultad para respirar, a veces necesitan oxígeno, eh retienen líquido, es decir, hay como una inflamación, el paciente como que se
hincha, ¿de acuerdo? Y hay veces que necesitan apoyo de oxígeno y si no somos capaces de oxígeno, pues a veces necesitan estar en la UCI con un soporte de un ventilador, ¿vale? De acuerdo. Incluso a veces algún paciente hay que intubarlo. Eh, esto eh generalmente ocurre eso en los primeros días. Hay pacientes que lo hacen muy rápido, a lo mejor en el tercer, cuarto, quinto día, pero sin embargo hay pacientes que a lo mejor lo hacen más tardíamente. ¿Vale? Para que nos hagamos una idea, los grados severos pues pueden aparecer alrededor del 20
25%, una cosa así. ¿De acuerdo? Vale. Eh, la neurotoxicidad, la neurotoxicidad es el generalmente ocurre después de este síndrome de liberación de citocinas, aunque puede ocurrir por sí sola, ¿vale? Y el que ha desarrollado este síndrome de liberación de citocinas es probable que desarrolle cierto grado de neurotoxicidad porque no viene un poco por de la misma causa de esta inflamación que ocurre en el organismo y es muy variable. Puede ser desde que el paciente tenga un pequeño dolor de cabeza h a que el paciente eh pues a lo mejor tenga le
cueste hablar o tenga esta clínica como si tuviese un ictus, por decir así, para hacernos un poco o que incluso el paciente a veces pierde la conciencia, ¿vale? Y suele ser muy brusco, además. También hay que decir que estas formas muy graves eh son muy poco frecuentes, ¿de acuerdo? Y y también tengo que decir un poco de modo de tranquilizar es que con la experiencia lo que se sabe es que cuando tú tienes identificado un paciente que tiene mucho riesgo de desarrollar estos problemas, ¿no? En el momento que empiezan a ocurrir, nosotros
ya sabemos que si actuamos muy rápido lo cortamos y aunque lo desarrolle no pasan a tener estos eh grados tan severos ni tan importantes. Con lo cual, aunque al principio sí que vimos muchos pacientes, por decir así, que se ponían muy muy malos, eso cada vez está bajando porque eh actuamos mucho más rápido, identificamos el problema antes y ponemos los tratamientos de forma que lo cortamos antes de que vaya a peor, por decir así. sería ya una manera de prevención, ¿no? A modo de eh en algunos casos incluso hacemos
alguna medida de prevención, pero sí que más que prevención lo que se hace es identificar el paciente de alto riesgo y ponerle tratamiento precozmente, ¿vale? Vale. Para cortarlo de raíz, ¿vale? A ver, luego hay una cosa que eh eh claro eh esto es como en todo. Cuantos más tratamientos o cuantas más complicaciones tiene el paciente, por ejemplo, el paciente desarrolla estas complicaciones, tal, y tú le tienes que poner muchos medicamentos para cortar esa inflamación, generalmente son tratamientos inmunosupresores,
¿no? Y viene el tercer problema más importante, que generalmente suelen ser las infecciones. Si tú a un paciente le has tenido que poner muchos tratamientos para cortar estas inflamaciones más desgraciadamente las quimioterapias que ha recibido previas, etcétera, claro, ahí tenemos que el riesgo de infecciones pues es bastante alto en estos pacientes, porque además también tienen una bajada de defensas. Eh, a veces, aunque suene raro, a veces damos de alta al paciente eh a los 14 días y de repente a las 3 semanas empieza a necesitar
transfusiones, que suena un poco raro, ¿no? Pero bueno, sabemos que eso es consecuencia de toda esta efecto inmune que hemos provocado y producan pues eso, una bajada de defensas. Y entonces, pues eso, en estas en en los primeros dos semanas es este síndrome de liberación y neurotoxicidad y posteriormente son lo que llamamos las citopenias, bajada de defensas, anemia, que bajen las plaquetas y consiguiente de eso, eh, el riesgo de infecciones, que generalmente puede ser durante los primeros dos meses, sobre todo cuando es más peligroso.
Vale. Bueno, pues ya lanzando con la última pregunta, cuando te iba a preguntar por los esos signos de alarma, ¿no? Es decir, el paciente se va de alta, ¿qué signos de alarma hay que tener en cuenta? ¿No? Pues es un pico de fiebre, por ejemplo, eh qué cosas sí se deben sí se deberían de preocupar y a lo mejor pues acudir a urgencias, ¿no? Generalmente eh en cuanto a los efectos secundarios más específicos del CART, está sobre todo a largo plazo eh esta toxicidad neurológica, ¿vale? ¿De acuerdo? Eh, porque hay veces que puede
ocurrir hasta en las primeras en las primeras cuatro o canas y puede ser muy variable desde pues esto que a lo mejor nos dice el acompañante, pues es que le veo raro o veo a mi mujer rara, como que no me tal se ha desorientado, eh, cosas así que dices, «Uy, esto nosotros lo vemos cuando están ingresados.» Que muchas veces por eso cuando decimos que lo identificamos antes es que ya nos lo dice el familiar. Uy, hoy se levantó y me preguntó, ¿no? Y nosotros dijimos, «Uy, espera, ¿qué algo está pasando aquí?» No, pues esto, estando en
domicilio, pues son ese tipo de cosas que hay que vigilar. De hecho, siempre decimos que cuando se van de alta tienen que estar eh prácticamente 24 horas al día acompañados durante dos tr semanas después del alta para vigilar si ocurre algún fenómeno de estas características y si ocurre corriendo para el hospital. A lo mejor no es nada y seguramente no sea nada, pero por si acaso, ¿vale? Eso en cuanto a la neurotoxicidad, en cuanto a las infecciones, es un poco lo que venía diciendo antes, ¿no? Cuantos más problemas haya habido al principio, ¿no?
Más riesgo hay de que estas cosas ocurran, ¿no? Entonces, nosotros ponemos eh ya antibióticos profilácticos, ¿vale? Para evitar determinado tipo de infecciones. A veces los pacientes les tenemos que poner en el seguimiento inmunoglobulinas porque otro de los problemas es que los linfocitos B desaparecen y al desaparecer los linmoglobulinas. hay más riesgo de infecciones víricas. Entonces, tenemos que ponerles a los pacientes inmunoglobulinas cada cuatro o se semanas en función del paciente. Y básicamente son eso. Y los signos, pues
como siempre nosotros hablamos, eh, si uno se encuentra bien y tiene un poquito de temperatura, pues vigilamos, no pasa nada. Pero si hay algo que no va bien, algo raro, eh, fiebre no controlada, ese tipo de cosas, pues hay que acudir porque generalmente suele haber una infección por debajo y si se corrige y se coge a tiempo, no debería de dar mayor problema. Vale, luego también y ahora sí que eso, bueno, pues hay algunos efectos secundarios que claro, con el recorrido que tenemos ahora con los CAR empezamos a ver y se
empiezan a ver que son efectos secundarios más a medio largo plazo, sobre todo a nivel neurológico, ¿vale? que los pacientes tienen que conocer y discutir con con su médico, porque tenemos que ser conocedores de que pueden ocurrir hablando, hablamos ya a lo mejor a 6 9 meses, eh cosas así que pueden ocurrir algún trastorno y bueno, pues hay que discutirlo con el y y y conocer que que pueden o que pueden también ocurrir. Vale, vale. Bueno, pues yo creo que ya terminamos y y muchísimas gracias por aclararnos todas estas dudas, porque
creo necesario que pacientes y familiares pues que tengan esta información porque muchas veces pues se van de la consulta o les surgen dudas que hoy aquí en este encuentro virtual pues esperemos que que hayan quedado resueltas. Así que nada, de nuevo, muchísimas gracias y y nos vemos en futuros encuentros. Pues nada, muchas gracias a vosotros y eso siempre con estas cosas los pacientes que pregunten todo lo que tengan que preguntar, que no se dejen nada en la libretita porque luego esa pequeña cosa que está el room
es lo que peor va. Entonces, que pregunten todo lo que tengan que preguntar. Muchísimas gracias. Gracias a vosotros.