Ponente: Valentín Valdés Valiña
Desde Asotrame, y gracias a Pfizer y Roche, os presentamos el encuentro virtual con el doctor Valentín Valdés Valiña, hematólogo en el Complejo Hospitalario de A Coruña (CHUAC). Esta temática se encuentra dentro del proyecto Hablemos de Hematología. En nuestro canal encontrarás más encuentros relacionados con el proceso oncohematológico.
Transcripción del vídeo
Buenas tardes. Muchas gracias a los que estáis viendo este encuentro virtual que estamos grabando para su posterior difusión centrado en el papel de las pruebas diagnósticas en relación con el cáncer hematológico.
Me presento, soy Ivana psicóloga de Asotrame y somos la asociación gallega de personas afectadas por un trasplante de médula ósea y enfermedades oncohematológicas.
Y hoy nos reunimos con el doctor Valentín Valdés hematólogo en el complejo hospitalario universitario de Coruña para abordar un tema que para pacientes a veces resulta complejo como son las pruebas que se realizan previo a un diagnóstico oncohematológico. Realmente existe una gran variedad de pruebas que son necesarias antes de confirmar un diagnóstico y muchas veces pues no se entiende en qué consiste o el porqué de cada prueba, por ello hoy queremos ofrecer información clara y accesible sobre este tema.
Me gustaría antes de nada agradecer a Valentín Valdés por su colaboración de manera altruista y por compartir con nosotros su experiencia y conocimientos y por último también me gustaría dar las gracias a empresas farmacéuticas que han apostado por esta entidad como son Rocher y Pfizer y que han hecho posible este encuentro virtual.
Así que nada sin más dilación, cuando quieras, empezamos.
Pues muchas gracias yo eso soy Valentín Valdés soy uno de los hematólogos de del CHUAC en concreto y me pidieron dar esta charla sobre pruebas diagnósticas en oncohematología y bueno lo primero, Ay que no me quiere pasar las diapositivas.
Lo primero daros las gracias a vosotros ¿no? A Asotrame por permitirme dar esta charla porque a veces cuando yo estoy en la consulta pues a lo mejor no tengo el tiempo, no tengo la capacidad de poder expresarme todo lo bien que querría cuando explicamos estas pruebas y que yo creo que pues ayuda a que los pacientes puedan entenderlo bien y luego daros las gracias por el resto de trabajo que hacéis de información a los pacientes de ayudarles durante el ingreso y después del ingreso y siempre, bueno, los pacientes siempre están muy agradecidos con esto.
Entonces ya sin más dilación, esto es un poco de lo que quería hablar hoy, por la tarde. Voy a hacer una breve introducción, luego hablar de la analítica y de la médula o un poco en paralelo un poco en el mismo grupo por bueno porque son probablemente de las pruebas más importantes en oncohematología y sobre todo la analítica no que a veces pensamos es una analítica no es una prueba diagnóstica pues es probablemente la prueba diagnóstica más importante para nuestros pacientes, luego hablaremos un poco de la biopsia de las de las lesiones ya sea de un ganglio o de otro tipo de lesión, de las pruebas de imagen que más utilizamos, obviamente no vamos a hablar de la radiografía porque bueno se usa para muchas cosas y todos la conocemos pero si de algún unas como el TAC o el PET TAC y luego un par de pinceladas sobre otras pruebas.
Entonces antes de nada quiero decir que van a ser explicaciones sencillas que no quiero profundizar mucho en algunas cosas, en otras a lo mejor sí que vamos a profundizar, pero que van a ser sencillas y generales a lo mejor no valen para todas las enfermedades. A lo mejor alguna enfermedad utiliza unas pruebas o tras otras, pero es para entender en general qué pruebas hacemos y qué y por qué las hacemos sobre todo no y por qué a veces empezamos a hacer, tenemos ya una prueba que nos dice un diagnóstico, pero esperamos a tenerlas todas.
Para entender un poquito todo esto. Entonces, bueno, si hablamos de pruebas complementarias o diagnósticas oncohematológicas. Tenemos que hablar de cómo llega el paciente a un hematólogo a una consulta de hematología y puede ser de varias maneras. Puede ser porque el paciente va al médico de cabecera y le ve que el médico de cabecera ve una alteración en el análisis o que tiene unos síntomas que le pueden dirigir hacia nuestras consultas y nos avisa y lo citamos en las consultas, puede ser que el paciente se hace una prueba por otro motivo y en la prueba, pues sale la biopsia, pues que tiene tal enfermedad hematológica y nos lo mandan. Y puede ser que el paciente pues lo que sea se encuentra muy mal va por urgencias y ya es en ese primer contacto el que tenemos que verlo pues porque tiene unos síntomas fuertes o graves, por desgracia, y tenemos que ingresarlo con el tratamiento.
Y esto, nos lleva diferentes tiempos en las pruebas en el paciente que viene desde el médico de cabecera desde otro especialista, pues probablemente podamos tomarnos lo más con calma en el sentido de comenzar el proceso de diagnóstico, hacer las pruebas en un digamos, que en una escalera, no primero una, luego otra, luego otra en el paciente que ya viene con un con un diagnóstico dado pues tenemos que completarlo ponerle los apellidos y hacer lo que llamamos el estadiaje ver hasta dónde llega la enfermedad. Y en el paciente que viene por urgencias, que tiene que ingresar muchas veces el tratamiento se tenemos que hacer un diagnóstico paralelo al tratamiento, es decir una vez que estamos haciendo las pruebas, pues ya pon un tratamiento para que la enfermedad no avance en nuestras narices. Y todo esto ¿por qué? Pues porque tenemos dar el diagnóstico más completo posible, yo siempre le digo a los pacientes, bueno Yo me dedico al área de diagnóstico sobre todo, pero llevo una consulta de síndrome mielodisplásico y siempre le digo yo es que quiero ponerle el nombre y todos los apellidos posibles que quiera encontrar en la enfermedad, que si yo conozco todos esos apellidos, cuanto más yo, cuanto más conozca yo la enfermedad pues probablemente el tratamiento pues sea más adecuado ya sea el tratamiento que llamamos convencional, el habitual, o encontrar una diana terapéutica, es decir un fármaco que va contra esa enfermedad en concreto, o en el caso de que necesite ir a un ensayo clínico.
Nos vale también para hacer un seguimiento preciso, cuanto más conozcamos la enfermedad, después de poner el tratamiento podremos encontrar mejor esa enfermedad o los restos que quedan qué es lo que se llama enfermedad mínima residual y nos vale para marcar un pronóstico que son las diferentes clasificaciones o categorías de riesgo que utilizamos. ¿Y todo esto con qué objetivo? Pues con el objetivo ofrecer a los pacientes el mejor tratamiento en cada caso y darle toda la información que ellos puedan necesitar. Y esto es un ejemplo y no me quiero parar mucho pero sí que quiero que veamos un ejemplo de cómo ha cambiado las cosas en la mitología y probablemente en muchas otras áreas de la medicina. Y es que antes se sabía que la gente que tenía, pues un tipo de células en la sangre que crecían de más, que yo les llamo células de las defensas que crecen de más, se tenía una leucemia aguda. Pero luego se vio más adelante y dijeron, pero es que este este grupo de pacientes, pues unos van, unos necesitan un tipo de tratamiento y otros de otro y además sus células, cuando las vemos al microscopio son diferentes. Y entonces dijo, pues esta se parece más a los linfocitos pues es una leucemia aguda linfoblástica y todas las demás pues son no linfoblástico.
Luego vino el grupo francés-americano-británico y nos dijo, pero es que dentro de la no linfoblástica hay todos estos subgrupos en función de cómo los vemos al microscopio. Es que luego llegó la genética y llegó la genética para quedarse y nos explicó que las enfermedades son diferentes porque hay un proceso genético detrás diferente ¿no? porque hay una mutación que hace que la que la enfermedad actúe de cierta manera. Y entonces la OMS nos dijo pues la leucemia aguda tiene todas estas categorías, en 2008, en 2016 nos dijo y tiene todas estas otras y hay que clasificarlo de tal manera y en 2022 nos dijo y hay todas estas otras ¿no? y luego en 2022 aparte aparecía otra clasificación distinta de otros expertos que nos dijo que mejor clasificarlos de esta manera ¿no? esto no es para que os quedéis con ello, pero sí para que veáis pues nuestra sensación al tener que diagnosticar a un paciente, que es necesitamos muchísima información, que cuanto más sepamos mejor vamos a organizar el tratamiento y es que es todo eso que os puse solo hablando de leucemia mieloblástica aguda que es un tipo de leucemia y no de todas las otras enfermedades hematológicas que tenemos. Hay un montón de grupos. Hay un montón de subgrupos y necesitamos encontrar la manera de mejor diagnosticar esa enfermedad para mejor para dar un mejor tratamiento. Necesitamos pruebas potentes para adecuar el tratamiento, poder hacer un seguimiento preciso y marcar un pronóstico y todo ello para ofrecer el mejor tratamiento y dar la mayor información al paciente, es decir yo pongo todas las cartas sobre la mesa al inicio para luego si necesitamos más tratamientos o no necesitamos, pero poder adecuarnos lo mejor posible.
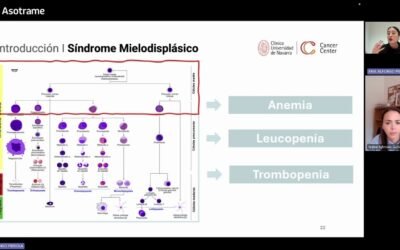
Entonces vamos ya con el contenido de la charla, vamos a hablar de la sangre periférica y de la de la medula ósea un poco en conjunto. Y si hablamos de sangre periférica pues tenemos que hablar de lo que más nos gusta a los hematólogos por así decir lo que son las células de la sangre, los glóbulos rojos, las defensas, las plaquetas, lo que llamamos el hemograma y así es como se ve en el SERGAS un hemograma y nos permite cuantificar las células de la sangre nos las clasifica y nos las cuantifica y habrá parámetros dedicados a los glóbulos rojos, parámetros dedicados a las plaquetas, parámetros dedicados a las defensas, entre comillas, porque defensas hay muchas, pero nos permitirá saber lo que está ocurriendo, pero yo quiero dejar claro una cosa ya en este punto de la charla: Y es que las causas más frecuentes de las alteraciones no son oncohematológicas, no son patológicas oncohematológicas. La causa más frecuente de alteración en un hemograma probablemente sea tener las defensas altas por una infección o tener anemia por tener el hierro bajo ¿no? Entonces no vayamos a la App del SERGAS a mirar nuestra analítica y decir Uy tengo un asterisco que estoy muy mal, no es así, pero sí que en nuestro caso es muy importante el hemograma. Y es que el hemograma nos habla de, por ejemplo, cuando tenemos los glóbulos rojos bajos pues tenemos anemia, cuando tenemos los las defensas bajas tenemos leucopenia. La anemia se produce en cansancio, la leucopenia riesgo de infecciones y la trombocitopenia que es tener las plaquetas bajas se traduce en sangrados. Así a grandes rasgos, pero puede ocurrir lo contrario que tengamos muchos glóbulos rojos que es lo que se llama poliglobulia y se asocia se asocia a picor o a riesgo de tener un trombo, leucocitosis que es tener muchas las defensas muy altas y se asocia una cosa que se llama síndrome de hiperviscosidad que no vemos entrar en ello o tener elevación de plaquetas y que se asociada también al riesgo de tener trombos.
Y volviendo a otro ejemplo, pues esta analítica, que no nos vamos a parar en ella, pero lo que tenemos es un aumento de las defensas, una anemia y una baja de plaquetas y es una persona que fue diagnosticada después de una leucemia mieloblástica, es una enfermedad que tenemos que tratar rápido y que tenemos que tratar de forma potente, pero este paciente que tiene una subida de defensas y que tiene anemia tiene una leucemia neutrofílica crónica, que es otra enfermedad totalmente diferente, que no hay que correr para poner un tratamiento y este otro tiene incremento de defensas y tiene una leucemia mieloide crónica, que es otra patología que pues también tiene un tratamiento muy específico y que se cura, bueno, en la mayoría de los pacientes y esto es otra enfermedad que muchas veces no hay ni que poner tratamiento y que también se manifiesta de la misma manera y esto es otra enfermedad que bueno que algunos tienen que poner tratamiento y otros no. Entonces, es decir, si todas las analíticas se nos parecen que todos tienen una elevación de defensas ¿Cómo diferenciamos una enfermedad de otra? La propia analítica nos ayuda y lo que hacemos nosotros es coger una muestra de sangre y verla al microscopio, la extendemos en un cristal y la vemos al microscopio y ahí podemos valorar la forma de las células categorizarlas correctamente y también ver si tienen alteraciones si tienen cosas que no deberían, si hay células en la sangre que no deberían estar ahí y es, bueno, un poco lo que nosotros vemos ¿no? y lo vemos así con un microscopio y vamos categorizando las en las diferentes formas de las células los diferentes, bueno, las diferentes categorías de las células y nos permite pues en los casos de antes, pues diferenciar, Por qué cada una de las enfermedades es diferente si lo que teníamos era un incremento de defensas. Y ahora, bueno, menos mal porque nos ahorra muchísimo tiempo tenemos programas que lo que hacen es fotos a las células y nos las clasifican y nosotros tenemos que revisar y ver lo que está ocurriendo, más que simplemente mirar el microscopio, estar bastante tiempo mirando y buscando una célula una a una y tal, nos ahorra bastante tiempo pero no todo es el frotis y podemos hacer otras cosas de la sangre, podemos hacer lo que se llama un inmunofenotipo, que es a lo que me dedico yo en concreto, no me quiero meter en esto que podría estar hablando varias horas solo de esto, pero sí que explicar un poco qué es y lo que es que mediante un programa informático analizamos las células y nos ayudan a diferenciarlas de las normales de las patológicas que vemos, no vemos la forma, vemos su composición, vemos qué proteínas tiene y aparte nos permite analizar muchas más células a la vez, con el frotis veíamos entre 100 y 500 y aquí podemos llegar hasta 10 millones, y aparte como sabemos qué proteínas tiene la célula que estamos buscando y la célula que consideramos mala, pues podemos ver que si tiene tal proteína, pues nos puede servir para atacar a la célula tumoral o cancerígeno y nos vale de diana. Si yo conozco que la célula tiene tal proteína en su membrana o en donde sea si tiene tal proteína si yo tengo un arma contra esa proteína puedo atacar a esa célula y esto ha cambiado la manera de hacer hematología y oncología, bueno, un montón de especialidades, que es la inmunoterapia. Si yo puedo dirigir mi tratamiento solo a lo malo, pues no tengo que poner tratamientos tan agresivos y a lo mejor que pueden ser menos eficaces, obviamente esto es un concepto general y hay casos y casos, pero ha cambiado un poco la manera de trabajar.
Y así es como como el protocolo que se analiza y como se ve, pero bueno, no me voy a parar en esto. En general, el frotis nos habla de la cantidad de células, si hay de más si hay de menos y nos habla de la forma de las células si esta tiene, pues más un tamaño mayor, si la membrana lo que la rodea es diferente, bueno, y el inmunofenotipo nos habla de también de la cantidad y de la composición.
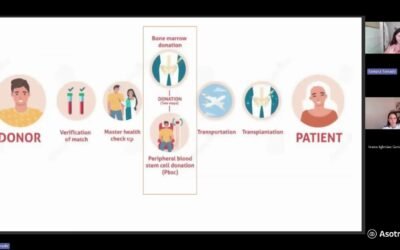
Y luego podríamos hablar de la genética que no voy a hablar aquí de la genética, luego ya hablaré un poquito más, pero sí que si habéis recibido un trasplante de médula ósea o vais a recibir un trasplante de médula ósea o tenéis algún familiar que está en ese proceso, pues probablemente os hagan esta analítica que es una analítica que mediante un estudio genético vemos si dos personas, sus médulas son compatibles y también que nos da muchísima información, nos ayuda a organizar los trasplantes, a buscar cuando no hay dentro de la familia, pues gente compatible fuera, es decir, es una de las pruebas en el trasplante de las más más importantes. No me voy a parar, pero simplemente para que sepamos que también se hace de una analítica que, a veces, consideramos que la analítica pues no es una prueba como las otras, pero luego volvemos a la genética.
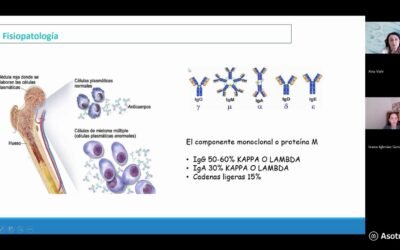
Sobre el estudio de la médula ósea, pues lo mismo, muchos de los que escuchéis esta charla a lo mejor habéis tenido que recibir esta prueba, y bueno, es una prueba que obviamente no gusta, es una prueba que si me preguntáis yo no puedo deciros si es dolorosa o no, tengo la experiencia de hacerla y de ver lo que se pueden quejar o no las personas y hay gente que le molesta mucho y hay gente que casi no le molesta n buen entonces en eso es un poco complicado decir pero sí que es una prueba muy sencilla. Es una prueba que se hace normalmente en una consulta o incluso en la cama de hospital, pero no tenemos que no tenemos que ir a un quirófano a hacerla y no tenemos que hacer, en general, anestesia general que muchas veces, pues, tiene sus riesgos. Se pone anestesia local, se duerme bien la zona y con una agujita se coge un poco de líquido de dentro del del hueso, de este hueso, bueno, la zona de la cresta ilíaca del hueso de la pelvis o en el externo. En Coruña, en concreto, pues somos más, o sea la hacemos más en el uso de la pelvis, pero por costumbre más que por otra cosa, no por no porque una sea mejor que la otra. Y eso, se coge un poquito del líquido y un trocito del hueso y es tan poquito lo que se coge que no hace falta ni puntos ni hacer curas los días siguientes, simplemente pues una serie de recomendaciones como no hacer esfuerzos grandes mantener el apósito que se expone pues durante 24 horas y es molesta en el momento, pero luego en general no suele dar mucho dolor los días siguientes y por eso tiene muy poquitas complicaciones, lo que puede pasar es que se nos forme un hematoma o que nos sangre un poco, pero no una complicación grave o bueno, es excepcional una complicación grave. Es muy rápida, en el momento que se hace pues son 5 o 10 minutos y luego pues nosotros aquí lo que hacemos es observar al paciente tenerlo en la sala de espera otros 10 minutos y si va todo bien pues se puede ir para casa. Y nos da muchísima información y es que es verdad que nos da muchísima información porque nos da la parte sólida la que consideramos la biopsia de la médula ósea como tal, el trocito de hueso, y la parte líquida, que es como una analítica, es decir, lo que sacamos es como una analítica y podemos hacer lo mismo que la analítica. Sobre la parte sólida, pues los resultados nos los da otro compañero del hospital, anatomopatólogo que se llama y es clave muchas enfermedades son oncohematológicas, en especial los linfomas, puse aquí, pero bueno también otros como los síndromes mieloproliferativos, muchos otros, nos permite ver la arquitectura de la médula, ver qué células hay si hay, si hay de más, si hay de menos , etc y sobre la parte del aspirado, pues nos da muchísima información también que nos permite hacer poquito lo mismo que hacemos en la sangre: hacer un frotis verlo con un cristal al microscopio, que nos ayuda a diagnosticar sobre todo y hacer un seguimiento, hacer el inmunofenotipo lo que vimos de las proteínas de las células y nos ayuda también a diagnosticar, a clasificar y hacer un seguimiento muy preciso porque sabemos las diferencias entre las proteínas de la célula normal y de la célula enferma, entonces después de poner un tratamiento sabemos si quedan células enfermas o no y lo que es la genética, que, ahora sí vamos a ver. Entonces, qué son los análisis genéticos hablando en oncohematología, no en general, pero hablando en oncohematología los análisis genéticos son buscar mutaciones y dónde buscamos las mutaciones, pues nosotros podemos hablar de la genética germinal por así decirlo que son los genes que le damos de nuestros padres que determinan si tenemos los ojos azules o si tenemos el pelo rubio, por ejemplo, pero no vamos a hablar de eso, lo que nosotros miramos es general ya digo porque sí que hay estudios dedicados a esto en oncohematología, lo que miramos es lo que llamamos la genética somática que es mirar los las mutaciones que puede haber en las células tumorales o las células malignas, son mutaciones que no tenemos de nacimiento por norma general y aparecen a lo largo de la vida y nos permiten por una parte conocer y comprender por qué se produce esa enfermedad en concreto y por otra pues nos ayudan a clasificarla y a dar un pronóstico y a buscar gras terapéuticas como veremos y se pueden hacer un montón de cosas: se puede mirar qué forma tienen los cromosomas si hay de más si hay de menos si hay dos cromosomas que se han fusionado entre ellos y están haciendo, pues que la enfermedad aparezca, si hay una mutación en un punto concreto del ADN, eso a día de hoy se puede hacer y se pueden encontrar pues un montón de cosas. Y cada día más y cada día va a estar más en auge y nos ayuda a eso, pues nos ayuda al diagnóstico y a la clasificación. Todas esas listas que os puse al principio están basadas todas en la genética a día de hoy o casi todas, nos ayuda al pronóstico porque se sabe que hay enfermedades dentro del mismo grupo que tienen esta mutación y responde mejor al tratamiento y estas otras que tienen esta mutación y responden peor. Nos ayuda al tratamiento porque yo sé qué, y esto es un concepto también un poco con pinzas, si yo ataco a la mutación, estoy atacando a la enfermedad, es decir, yo comprendo cómo funciona la mutación. El cuerpo si sigo un fármaco que hace que eso no funcione así ataco la enfermedad y lo mismo nos ayuda el seguimiento si yo después del tratamiento sigo detectando esa mutación es que la enfermedad sigue ahí porque como decíamos son mutaciones que tenemos en las células malignas solo, no las células de todo. Y este probablemente sea el mejor ejemplo, o en mi opinión vamos. La leucemia mieloide crónica es una patología que se genera porque unos genes del cuerpo se fusionan entre ellos y hacen una proteína, que esa proteína lo que hace es que la célula sobreviva, sobrevive tanto que se convierte en mala y nos hace daño. Entonces, antes ¿qué se hacía? el trasplante de médula o lo que estos pacientes se curaban a base de trasplantar la médula a otra persona y eliminabas la mutación, ahora lo que se sabe, esto ya tiene tiempo, no sé ahora recientemente es que tenemos un tratamiento que va contra esa proteína, hace que esa proteína no funcione y elimina la enfermedad y con un tratamiento, que son unas pastillas, que se toman, pues una vez al día, estamos como si no tuviésemos nada. De forma general, hay pacientes que van mejor, peor, pero que como si no tuviésemos nada y no tenemos que pasar por un trasplante con todas esas ventajas que conlleva no tener que pasar por el trasplante, pues: ingresos largos, tener que buscar donante etcétera.
El problema de la genética a día de hoy, pues siendo sinceros, no tenemos los resultados inmediatamente, a veces tardan semanas en el mejor de los casos, a veces tardan meses, por eso, muchas veces no esperamos a los tratamientos. Y luego adecuamos el tratamiento en función de lo que nos salga en la genética. También, el problema, que no conocemos todos los genes implicados, ni el significado de todos ellos, a veces encontramos una mutación en un gen y no sabemos interpretarla y nos trae un poco por el camino a la amargura. Tenemos, que, necesitamos más estudios en muchos genes y no todos los genes nos aportan dianas terapéuticas, no hay fármacos para todas las dianas y algunos fármacos que estaban pensados para ser dianas, pues a lo mejor no demostraron ser tan útiles como parecían. Entonces, es un campo en investigación y bueno hay que seguir ahí y seguirá probablemente.
Y luego ya, entrando en otro tipo de pruebas fuera de la médula ósea y de la sangre pues hablar de la biopsia ganglionar u otras lesiones que es como se diagnostican en general los linfomas y hay varias maneras de hacer una biopsia. Yo aquí puse las dos principales que es la biopsia excisional que es quitar la muestra entera, es decir, si tenemos un ganglio, quitar el ganglio entero, si tenemos una lesión, por ejemplo, en la barriga, pues quitarla, o la biopsia guiada por imagen, que lo que hacen es, se hacen una ecografía o un TAC y con una aguja que se llama gruesa pero que es una aguja a fin de cuentas cogen una muestra de la lesión. ¿Y qué diferencias hay? por la biopsia excisional se hace en un quirófano normalmente lo hacen, los de aquí en Coruña, los cirujanos generales o los otorrinos, normalmente, que puede requerir anestesia general en función de dónde esté localizada y en general es más agresiva que la otra porque si hay una lesión que es más interna. Pues a lo mejor hay que hacer cirugía más grande etcétera, pero nos da mucha información porque tenemos la lesión completa la biopsia con aguja gruesa guiada por imagen, pues es más accesible siempre que haya profesionales formados, en general, son radiólogos, son los mismos que hacen el TC, que te hacen la ecografía, son los que te hacen la biopsia. No requiere anestesia general por norma general y es menos agresiva porque si tenemos una lesión por así decirlo interna, que no es como un ganglio que tenemos en el cuello, sino que tenemos algo en la barriga que no se puede llegar con cirugía o con cirugía menor. Por así decirlo, pues con la aguja así que llegan y nos dan información, pero sí que la información no siempre es suficiente y a veces pues dependiendo del caso hay que usar una prueba u otra porque si nosotros nos vamos al microscopio, cogemos la lesión y nos vamos al microscopio después de quitarla la excisional nos da la lesión entera y la aguja gruesa nos da solo un trocito de la lesión. Entonces nos da menos información, que a veces, es suficiente pero no siempre, entonces, hay que adecuar a la prueba pues en función de cada caso.
Y luego, ya hablando de pruebas de imagen, pues ya os dije, no vamos a hablar de la radiografía ni de la ecografía probablemente porque son muy conocidas por todos ya fuera del ámbito de la metodología, pero es que vamos a hablar del TC. El TC es un cómo hacer muchas radiografías, radiografías en muchos sitios o sea de seguido al pasar por ese por ese aro que aparece ahí, y nos da una imagen del cuerpo por dentro. Nos permite buscar dónde encuentran las lesiones, saber dónde hacer una biopsia, por ejemplo, o si sabemos que tenemos una lesión aquí en el cuello, pues vemos en qué más sitios hay. Nos permite marcar un pronóstico eso que llamamos estadiaje y nos permite planificar el tratamiento, es decir, pues si solo está en, pues esa lesión en el cuello, a lo mejor podemos dar un tratamiento localizado, pero si está en más sitios, que, por desgracia, es lo más habitual por ejemplo los linfomas, tenemos que dar quimioterapia. Nos permite hacer un seguimiento también porque si tenemos un TC antes de empezar el tratamiento y otro después vemos cómo ha cambiado, si han desaparecido las lesiones o si han crecido, si han desaparecido, pero no del todo, bueno, eso nos permite hacer un seguimiento. Eso tiene la ventaja de que es rápida, casi todos los hospitales tienen un TC y nos da y no suelen tener mucha espera, en general, sobre todo en estos casos de enfermedades oncohematológicas y luego tienen otros usos como buscar infecciones u otras enfermedades. ¿Cómo se ve? pues vemos esto, digamos, que son lo que llamamos cortes en los diferentes puntos en los que ha pasado la máquina de TC y nos dan diferentes imágenes y tú puedes ir subiendo, bajando ver cómo se relaciona una estructura con otra, ver bueno, nos da mucha información en ese sentido. Y luego el PET/TC, es una mezcla de dos tecnologías: El TC que es lo que vimos con el PET, que es una técnica, que lo que utiliza es un radiofármaco, que radiofármaco es una palabra muy rara, pero básicamente es un azúcar marcado. Es un medicamento que es de base de azúcar y los órganos que más consumen azúcar, pues ese ese azúcar irá a ellos y no solo los órganos también los tumores, que como necesitan mucha energía, pues gastan mucho azúcar. Entonces las imágenes que tendremos, pues nos da este azúcar dará una señal en las zonas, donde, pues más actividad hay. Entonces, los tumores como tienen mucha actividad, pues se verán zonas muy activas y aparte no solo si son más activas o no, podemos mirar cuánto de activas están, entonces podemos ver cómo vamos respondiendo al tratamiento. Si hacemos un PET/TC al inicio y, esto es un número sin venir a nada, pero, decimos que está activa a un cinco y luego está activa un uno es que tiene menos actividad y va mejor o activa cero, es que bueno, que ya no está activo, pero bueno es un número de ejemplo no que tiene que ver con ninguna enfermedad y eso nos permite hacer un seguimiento. Y así es como se vería, pues como una imagen de TC y es la última de las tres imágenes y si nos fijamos en el circulito azul, pues tiene muy poca captación porque está muy azul, lo de dentro está con poco naranja y en el circulito rojo que es una lesión que sí que capta más pues tiene más naranja, pues así es como lo vemos, esa lesión más fuerte pues consume más azúcar y entonces somos capaces de verlo.
Luego ya, pues, la resonancia, que tiene la ventaja con respecto a las otras dos pruebas que no produce radiación, es por así decirlo inocua, menos agresiva, pero que no es la prueba más importante en hematología. Es muy útil para descartar cuando una enfermedad nos puede afectar al cerebro, a la médula espinal, pero poco más, en general en hematología. Y, además, tiene ciertos problemas que es sobre todo, una prueba lenta hay que estar mucho tiempo ahí tumbado, la máquina tiene un alto coste y todos los hospitales tienen acceso a ella, pero no siempre está en el propio hospital en el que en el que nos están tratando, nos están diagnosticando, es difícil de, a veces de interpretar y necesitan radiólogos muy bien formados para interpretarla y luego para el paciente pues que puede generar claustrofobia porque es mucho tiempo metidos en la máquina y luego que, como funciona por magnetismo no la por radiación no admite materiales metálicos y por ejemplo la gente con marcapasos pues no la puede usar.
Y luego, otras pruebas ya para acabar, la punción lumbar, por ejemplo nos ayuda a mirar el líquido que rodea el cerebro y la médula espinal y nos permite, que no tiene nada que ver con la punción de médula ósea, pero a veces por los nombres nos confundimos y nos permite mirar el líquido del cerebro, o sea, mira si hay afectación del cerebro y la médula y nos permite también poner tratamiento porque de la misma que quitas el líquido pues si hay enfermedades que necesitan tratamiento a ese nivel pues lo podemos poner. Y luego la toracocentesis o paracentesis que básicamente es quitar líquido del pulmón o sea de la de la cavidad que rodea el pulmón más bien y del abdomen pues lo mismo, nos permite dar diagnósticos de si esa zona está afectada por las enfermedades y nos permite aliviar los síntomas, también, pues en esas personas que tienen mucho líquido y les está, por ejemplo, no les deja respirar bien.
En definitiva, tenemos un montón de pruebas y todas las pruebas pues a lo mejor no todas en una enfermedad en concreto, pero todas las pruebas son necesarias y a veces tenemos que esperar el resultado de todas ellas o de muchas de ellas para un diagnóstico preciso y poder darles un tratamiento dirigido a los pacientes con el objetivo de tener los mejores resultados posibles.
Nada más, muchas gracias y quedo a disposición tuya para todas las preguntas que tengas para hacerme.
Muchas gracias, Valentín, sí que es cierto que tengo unas cuantas preguntas de pacientes, creo que algunas más o menos ya se han comentado, pero bueno, ahora las explicamos con mayor detenimiento
La primera, por ejemplo, de las pruebas que presentaste hoy realmente me preguntan ¿Cuál es la que tiene un mayor riesgo o, a lo mejor, la que tiene los efectos secundarios más adversos? Bueno pues probablemente riesgos, pues todas tienen porque al final en medicina todas las pruebas y tratamientos tienen ciertos efectos secundarios, pero a lo mejor la biopsia excisional si es una lesión que no se puede acceder muy bien a ella, pues tiene más riesgos, pues el riesgo de si tenemos que llevar una anestesia general, el riesgo de al final una operación. Luego efectos secundarios, pues eso, pues probablemente eso, sí que es verdad que a lo mejor cuando nos viene a la cabeza la biopsia de médula ósea pues muchos pacientes se asustan mucho, bueno porque al final pues es anestesia local y el paciente en la mayoría de los casos está despierto, entonces a veces pues es molesta, siente dolor, pero en efectos secundarios, por ejemplo, no es tan complicada o difícil, de hecho, los efectos secundarios de esa prueba son mínimos. Entonces, bueno yo diría que más hacia las biopsias de ganglios o cosas así dentro de que también son seguras, que no quiero desmerecerlas.
Bueno, un poco ya relacionado entonces con la segunda pregunta, ¿realmente me preguntan qué tan doloroso o incómodo puede ser la biopsia de médula ósea? si se necesita la anestesia o algún tipo de preparación previa y también preguntan Qué debo hacer si tengo dolor o efectos secundarios después de la biopsia. Pues mira de la de cuánto doloroso es es un poco lo que dije, yo a lo mejor no soy quién para juzgarlo porque no la he recibido y entonces a lo mejor alguien me escucha y dice pues no tiene ni idea porque a mí me ha dolido muchísimo, pero sí que es verdad que la experiencia haciéndola tú ves gente de todo tipo y hay gente que le duele mucho, hay gente que no le duele absolutamente nada, y al final también influye mucho como de entre comillas preparados vamos, pues hay gente que ya viene muy nerviosa y nos duele más cuando nos la hacen y hay gente que está más tranquila y les duele menos. Yo siempre digo lo mismo, y es una tontería, pero bueno, siempre me gusta explicarlo así, a mí por la anestesia que te voy a poner cuando te hago la prueba, no me van a cobrar, entonces si te duele me avisas y ponemos más porque no es a mí a quien le está doliendo ni a quien le están haciendo la prueba. Entonces, yo voy a poner la que yo considero, pero si a ti te duele me avisas. Y, si necesito algún tipo de preparación? En general no, hay gente que, pues eso, que es más nerviosa y a veces se toma un ansiolítico antes de venir a la prueba, pero bueno eso siempre como cualquier medicamento, con cabeza y bajo supervisión. No un ansiolítico y que te lo tomes si nunca lo has tomado antes porque luego puede tener el efecto contrario. Y luego si tienes efectos secundarios después de la prueba? Pues ahí ya depende de qué efecto o sea qué efecto secundario, qué síntomas puedes tener, pues cuando hacemos la prueba es normal que después, pues en el apósito que ponemos, en la gasa que ponemos, quede un poquito de, una gotita de sangre o así que sangre un pelín. Si ese apósito se empapa de sangre eso ya no es normal, es decir, si hay un poquito de sangre pues es normal, si se empapa de sangre pues no. A lo mejor hay que ir al centro de salud o a urgencias si vemos que sangra mucho. Un poquito de dolor los días siguientes también, pero si pasa una semana y sigues con mucho dolor, pues consulta con tu hematólogo porque, bueno, probablemente no sea nada, pero tampoco es normal, entonces son estos efectos secundarios que estoy diciendo son muy poquito probables o sea yo casi no los he visto pero a veces ocurren. Entonces, si vemos que la gasa que ponemos está muy manchada de sangre o al día siguiente cuando nos duchamos y nos la quitamos sigue babeando sangre la herida, pues a lo mejor sí que hay que consultar, ya sea eso urgencias o el médico de cabecera y lo mismo con el dolor. Un dolor unos días después que se calma con paracetamol o algún analgésico pues es normal, pero si nos duele mucho y sobre todo si se mantiene en el tiempo pues eso ya no es normal y a lo mejor hay que comentarlo con, pues ya digo, el médico cabecera o con el hematólogo principal de nuestro caso. Al final todos tienen un hematólogo de referencia.
Preguntan también si hay restricciones en dietas o algún tipo de medicamento o actividades físicas, por ejemplo, antes o después de alguna de las pruebas que hemos comentado hoy. Vale, pues bueno, esto depende un poco de qué prueba y a ver si hablamos del PET-TC, por ejemplo, del TC no, pero del PET-TC, pues como sí que utiliza azúcar, lo que expliqué no es radiofármaco que es azúcar marcado entre comillas, si hemos comido las horas previas, pues la prueba se va a estar refractada porque hemos comido azúcar a través de las diferentes comidas. Entonces, normalmente cuando nos avisan para hacer el PET- TC, pues nos dicen en tal fecha vas a ir, pues ya dan una unas recomendaciones desde allí, pero normalmente creo que es y aquí me puedo equivocar porque eso lo hacen los radiólogos, creo que son 6 horas antes estar en ayunas y los diabéticos, bueno la gente diabética, pues tiene una serie de diferencias. Y luego de medicamentos o actividades físicas, pues sí que después de, o sea que antes de la médula ósea, de cualquier biopsia, ya sea de un ganglio o lo que sea, pues si estamos con un anticoagulante, pues no se puede hacer porque hay más riesgo de sangrado, pero, lo mismo, normalmente al menos aquí desde el CHUAC tenemos protocolos y cuando citamos a los pacientes ya se les avisa de cuándo quitar el anticoagulante tantos días antes o el día antes o si no hace falta, bueno eso normalmente ya lo organizamos. Yo, lo de siempre si tienes dudas de si puedes tomar ese medicamento o no antes de la prueba, pues cuando te llamen para la prueba o pues preguntas o sea yo creo que lo más fácil es preguntar porque, a veces, bueno, pues nosotros vamos con prisas o asumimos que cosas son normales y pues a lo mejor no lo decimos, pero si tú tienes dudas de estoy tomando tal medicamento, pues nos preguntas y salimos de dudas que al final es lo más más sencillo. Totalmente de acuerdo.
Preguntan también si es posible que los resultados de una prueba no coincidan con los de otra y si esto es así ¿Qué significa el que no coincidan? ¿qué explicación hay a esto? esa pregunta es más más complicada de responder, pero si, es, bueno, no voy a decir que es frecuente, pero es bastante posible que haya resultados que no coincidan y eso nos lleva lo que nosotros desde hematología, y, probablemente otras especialidades llamen el diagnóstico integrado, es decir, cogemos los resultados de la médula ósea, del inmunofenotipo y los de la sangre y los de la biopsia del ganglio, y hacemos, bueno, el hematólogo en concreto que ve a cada paciente, pues integra todos los datos y dice, pues aunque este estudio pues parezca que sea tal enfermedad, en realidad todos los demás apuntan a esta y es habitual porque al final con cada prueba estamos viendo una parte de la enfermedad, no lo estamos viendo en su conjunto, entonces integramos todo. Es, normalmente, lo más habitual es que todo coincida, pero es posible que no y a veces eso pues, bueno, al final el médico que lleva a cada paciente, pues es el que tiene la última palabra y el que integra los datos. Y a veces si no coincide exactamente pues, o hay que repetir pruebas o hay que, ponemos el tratamiento y luego vemos y repetimos las pruebas después del tratamiento y vemos si algo se asocia o no, bueno, al final, hay que coger la enfermedad en conjunto y todas las pruebas en conjunto, no es que una mande más que otras, en algunas patologías sí. Si hablamos de leucemia, por ejemplo, la prueba de la médula probablemente sea la más importante, pero hay que coger, dentro de la médula, pues cada estudio de los que podemos hacer, pues unirlos y dar un diagnóstico en común, que, últimamente, pues con tantas pruebas y con tantos estudios, cada vez se hace más complicado, pero en beneficio de los pacientes para que tengamos el diagnóstico más preciso.
También me preguntan ¿cuántas pruebas serán necesarias para confirmar el diagnóstico de manera definitiva? Pues un poco más de lo mismo, eso es complicado y depende de qué enfermedad, pues si hablamos, por ejemplo, de un linfoma, pues le hacemos una biopsia del ganglio y nos da ese diagnóstico y ese diagnóstico debería ser definitivo, pero es que luego hacemos un montón de pruebas más para saber hasta dónde llega ese linfoma, esto es un ejemplo. Si es una leucemia, pues lo mismo hacemos la médula, pero es que a lo mejor hacemos dentro de la médula varias pruebas o más pruebas, entonces, ¿cuántas pruebas? depende del caso y de la de la enfermedad, pero probablemente, pues varias. En todos vamos a hacer una analítica, en casi todos vamos a hacer un estudio de medula ósea, y luego, en función de los resultados pues a lo mejor vamos haciendo una u otra, pero, y luego es eso, que dentro de cada prueba por así decirlo hacemos varios estudios. Entonces, al final, pues decir un número pues es muy complicado y como buen gallego voy a decir que depende del caso.
Preguntan ¿Qué debo hacer si mis síntomas empeoran antes de que tengamos todos los resultados, antes del diagnóstico? Pues muy buena pregunta también, aquí pues bueno, depende del manejo que tengas en tu consulta y las posibilidades, pero si tú te encuentras mal, sobre todo, pues si cada vez, pues estás más deteriorado, tienes más cansancio, sobre todo fiebres o pues falta el respirar, que nos falta el aire, lo que sea, pues ir a urgencias. Si me encuentro tan mal que no puedo hacer mi vida normal, bueno, mi vida normal o la vida que estaba haciendo hasta ese momento, ir a urgencias, pero sobre todo con fiebres, falta de aire, etcétera. Si estamos cerca de la consulta con nuestro hematólogo, pues consultarle a él aunque falten resultados, si yo me encuentro, si, aunque vaya a la consulta del hematólogo, si yo me encuentro mal, y no tengo, o sea, y aún no están las pruebas, pues a lo mejor desde el hematólogo sí que me puede dar un tratamiento puente o puntual para mejorar mi situación antes de tener un tratamiento definitivo. Entonces como siempre comentarlo, no callarnos información por ninguna de las dos partes, por así decirlo y buscar una solución, pero ante la duda si nos encontramos muy mal, a urgencias.
¿Hay algún tipo de resultado en particular que podría cambiar el plan de tratamiento ante una neoplasia hematológica? Sí, aquí es, muchas, o sea, ocurre, no cambia el tratamiento en general o el tratamiento que estamos llevando, pero sí el plan general, y era lo que comentaba antes con la genética. La genética nos tarda semanas e incluso meses dependiendo de qué tipo de estudio y a lo mejor tenemos que, pues, por ejemplo, una persona de esas que decía que viene por urgencia se encuentra tan mal y tenemos que ingresarla y poner un tratamiento antes de tener los resultados de la genética. A lo mejor el tratamiento es uno que, entre comillas, vale para todas las de ese tipo, pero luego un resultado de genética nos sale que hay una diana de las que podemos utilizar para tratar. Entonces, pues a lo mejor tenemos algún fármaco que va contra esa diana, entonces el primer mes a lo mejor ponemos tal tratamiento y luego a ese tratamiento le añadimos otro, pues eso lo mismo, depende de la enfermedad, pero sí que te puede cambiar, sí que las pruebas nos pueden hacer cambiar el plan global de la enfermedad y por eso hacemos tantas, por eso hacemos muchas, aunque algunas tarden, aunque tengamos que esperar por ellas.
Y ya la última, me preguntan ¿qué tan precisa es la biopsia de médula ósea para diagnosticar un tipo específico de cáncer hematológico? Pues eso depende, por ejemplo, si hablamos de linfomas, muchos linfomas no afectan a la médula ósea, la tenemos que hacer Igual, la prueba, o muchas veces la tenemos que hacer Igual, pero para asegurarnos de que está limpia, de que no tiene enfermedad ahí. Entonces, para diagnosticar un linfoma, yo diría poco específico, para diagnosticar, por ejemplo, una leucemia, pues es la clave, si no tienes un estudio de medula ósea, cuando hablo de biopsia, me refiero al estudio en general no solo la parte sólida como decía la charla. El estudio de médula ósea es en ciertas enfermedades muy preciso y sin ese estudio, bueno puedes pensar que es lo que está ocurriendo, pero sin tenerlo, no puedes confirmar el diagnóstico. A veces, a veces, entre comillas, falla a veces no tienes, no te da tantos datos como querrías, pero en general sin ese estudio, muchas veces no puedes poner un tratamiento definitivo, y en hematología, en casi todas las enfermedades es necesaria la biopsia, ya sea eso para confirmar el diagnóstico, o, para al menos, saber que la médula ósea no está afectada, que muchas de nuestras enfermedades se esconden allí. Entonces, es una prueba, yo diría que es de las más, la analítica y esa, de las más importantes para nosotros.
Vale, pues nada Valentín, me queda agradecerte, darte las gracias por explicarlo, además, de una manera creo que dinámica y sobre todo de un, con un lenguaje tan accesible que es algo que se agradece para los que no pertenecemos al ámbito hematológico. Entonces, muchísimas gracias por tu aportación y por tu colaboración.
Bueno, gracias, ya dije gracias a vosotras por contactarme, que la verdad, bueno, a mí hablar con los pacientes, que, si alguien me conoce y los que me ven, pues sabrá que me gusta y darles información y este tipo de cosas pues siempre ayuda, tanto a ellos como para nosotros porque cuanta más información haya sobre la mesa, pues mejor para todos.
Entonces, nada, muchísimas gracias a vosotros en realidad.