(1634) ¿Qué son los síndromes mielodisplásicos? – YouTube
Transcript:
(00:00) Buenos días. Os damos la bienvenida a este encuentro virtual en el que abordaremos los síndromes mielodis plásticos. Hoy se trata de abordar a qué nos referimos cuando el personal de hematología habla sobre este síndrome, ¿no? ¿Qué es, qué implica o o cómo se trata? Y todas estas dudas nos las responderá la hematóloga Ana Alfonso, que combina su faceta sanitaria con la investigación y y docencia.
(00:28) Antes de nada, agradecer Ana su colaboración e implicación en este proyecto Espacio Pacientes, ya que para Sotrama es muy importante eh ofrecer información de de mano de de la mano de profesionales cualificados, ¿no? Así que eh antes, bueno, pues cuando quieras, Ana, eh comenzamos. Bueno, voy a empezar compartiendo eh la pantalla a ver si supongo que se verá bien.
(00:58) Así que eh bueno, yo ya han explicado, soy Ana Alfonso, me dedico sobre todo al síndrome Merodis Plásico y antes de empezar me gustaría agradecer la oportunidad a Ivana y a Sotrame por estar aquí hoy grabando esto. Yo creo que ehimo que los pacientes conozcan su enfermedad y eh es la única manera en sobre todo en en el melodisplásico, desde luego, de entender por qué tomamos las decisiones que tomamos los los médicos.
(01:32) Así que yo paso mucho tiempo intentando explicarles a los pacientes qué es lo que tienen y qué es lo y qué es lo que vamos a hacer. Y hoy voy a intentar hacerlo, nunca lo había hecho con diapositivas, así que voy a intentar hacerlo así con unas diapositivas, ¿no? Y e voy a empezar un poco por eh voy a seguir un esquema, ¿no?, de introducción, diagnóstico, pronóstico y tratamiento.
(01:58) Eh, y en la introducción, para entender qué es el el medio bisplásico, tengo que empezar explicándoos qué es la hematopoyesis, ¿no? ¿Y qué es esto de la hematopoyesis? pues es eh es lo que en términos coloquiales decimos la fábrica de la sangre, o sea, es decir, es cómo se producen las células que tenemos circulando en eh en sangre, ¿no? Y todo esto empieza, ¿no? En eh en en la médula ósea, ¿no? Con esa célula madre e, perdón que voy a quitar esto ahora con esa célula madre hematopoyética, ¿no?, que es la primera célula, ¿no? más indiferenciada, que es la que es
(02:38) responsable de eh de todos sus hijas, ¿no? Que veis aquí que no es un esquema sencillo. Entonces, es esta célula madre la que da lugar a todas las células de la sangre y hay algunos tipos celulares que ya veis que está aquí seleccionado en amarillo, ¿no? Que solo los vemos en condiciones normales en la médula ósea y hay otros, ¿no?, que solo los vemos en condiciones normal, bueno, lo podemos ver en medula ósea, pero son las células que tenemos en sangre, que es las que conocemos eh todos más habitualmente.
(03:08) Bueno, pues esta célula madre es punto clave en esta en esta enfermedad, ¿no? Esta célula madre que da lugar a dos progenitores comunes, ¿no? Pues todo esto es punto clave eh en esta enfermedad, ¿no? Y hay como tres grupos celulares que son muy importantes, ¿no? que son el resultado de toda esta maduración de esa primera célula madre, que son por un lado los hematíes, que son los encargados de transportar el oxígeno que están aquí, los eh las plaquetas, que son los responsables, son los primeros que las primeras células que llegan cuando hay
(03:45) una rotura, ¿no? En un vaso, ¿no? Un sangrado, un corte o lo que sea, que son que están aquí, que es este último paso. Y por otro lado, ¿no? al final las los leucocitos o globalmente, ¿no?, lo que decimos las defensas, ¿no?, que es todo esto que tenemos a este lado de la de la diapositiva, ¿no? Y que eh que son las defensas, ¿no? Los que nos vienen a defender.
(04:13) ¿Y qué dónde está esto de la médula ósea? Porque la médula ósea no es una cosa que se pueda tocar, o sea, no es no todo el mundo entiende lo que es un pulmón, pero la médula osea es una cosa líquida, o sea, es un es un tejido líquido y está dentro de el hueso de los huesos, ¿no? De aquí donde haya hueso esponjoso, ¿no? Eh, tenemos medula.
(04:32) O sea, es lo que sería el tuétano del hueso, ¿no?, que les decimos a veces a los pacientes. Pero esto no siempre es así porque e en el en el desarrollo, ¿no?, antes de de nacer, nosotros somos capaces, ¿no?, nuestro los niños en cuando están en la barriga de sus madres son capaces de producir células de la sangre en otros tejidos como es el hígado o el bazo.
(04:55) Esto desaparece en el momento del nacimiento y toman posesión, ¿no?, de esa producción de esas eh de esa médula ósea y de esa producción de células sanguíneas, los huesos, ¿no? Como veis aquí, así por eso, ¿no? Eh eh en la edad adulta, sobre todo tenemos médula ósea en las vértebras, en el esternón, en las costillas, ¿no? O sea, que está la médula ósea está dentro de ese de de los huesos.
(05:23) Entonces, eh la médula ósea ya hemos dicho que produce todos los las células de la sangre. Por lo tanto, si la médula ósea está bien, también va a estar el hemograma bien. El hemograma es una prueba que realizamos todos los días. Cada vez que vais al médico y os sacan una analítica de sangre, siempre incluye un hemograma.
(05:44) Es una prueba muy sencilla que lo que hace es contar, ¿no?, las células sanguíneas. es decir, cuántos glóbulos rojos hay, cuántas de esas plaquetas que os he dicho antes hay y cuántos leucocitos hay. Tiene ya veis que hay algunos parámetros extra, ¿no?, que a veces nos ayudan a intentar diferenciar, ¿no?, por qué falta una cosa o la otra, pero en general es un recuento celular eh de todas esas células de la de de la de la médula ósea, ¿no? De esas células que produce esa célula madre hematopoyética.
(06:13) Y así cuando si la médula no está bien, nuestro hemograma tampoco estará bien y podrá haber anemia. Anemia llamamos la anemia puede ser de de múltiples causas, puede ser de de causa medular o puede ser por otras cosas, ¿no? Eh, pero si tenemos una anemia, ¿no? Que veis aquí, por ejemplo, en esta diapositiva, 6,4 de hemoglobina o unos hematíes bajos, pues esto, ¿cómo se va a representar? pues en un paciente que está cansado, ¿no? Si tenemos una unos leucocitos bajos, ¿no?, que tenéis aquí unos leucocitos eh 3280, pues tenemos lo que llamamos una
(06:46) leucopenia y esto eh se puede eh eh representar como un paciente que tiene infecciones, ¿no? Porque tienen le faltan esas defensas, luego tiene infecciones. Y por último, un paciente con plaquetas bajas, ¿no? Como tiene este paciente 90,000 plaquetas, se dice que tiene trombopnea, ¿no? y está más a riesgo de tener un sangrado porque son esas células las responsables de, no, como hemos dicho antes, de protegernos de las infecciones, de intentar evitar los sangrados y eh de transportar el oxígeno como es eh la hemoglobina.
(07:21) Entonces, el hematólogo una vez que no que tienes un hemograma, el médico de cabecera os hace un hemograma o vais a urgencias, os hacen un hemograma, a veces llaman al hematólogo que va a completar esos análisis de sangre y en caso de necesario, si quiere ver cómo está funcionando la médula ósea, va a hacer una punción de médula ósea, ¿vale? ¿Y qué es? No, ya os explicáos un poquito que es la hematopoyesis.
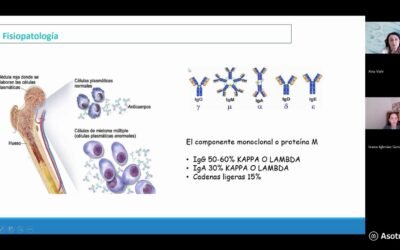
(07:45) Ahora tenemos que explicar qué es un síndrome mielodisplásico. Bueno, pues si vamos otra vez al mismo esquema, es un síndrome mielodisplásico, es una enfermedad tumoral o una neoplasia de estas primeras células, ¿no? De las más inmaduras, que hace que e las células maduras, esas que tenemos circulando en sangre sean defectuosas y además que mueran demasiado pronto.
(08:13) Entonces, al final yo siempre digo que es una médula que trabaja poco y mal, ¿no? Entonces, eso es lo que es un síndrome miodobisplásico, una enfermedad neoplásica de estas primeras células que hace que no tengamos a disposición, ¿no?, buenas células y y muchas células, o sea, que tenemos muy poquitas células de estas en sangre periférica.
(08:35) Eso da lugar que los mielodisplásicos vayan acompañados de anemia, leucopenia y tromopenia, que es lo que os he dicho que veíamos en ese hemograma que hacemos en eh que hacemos por función de de la avena. Entonces, cuando hay una anemia, una leucopenia o una trombopenia que no se explica por un déficit vitamínico que no se explica, no, por cosas más sencillas, el hematólogo es cuando procede a hacer los siguientes estudios para descartar, entre otras cosas, un síndrome mirodisplásico, pero que puede ser muchísimas otras cosas. Así que los
(09:09) pacientes con síndromes melodisplásicos, si no tienen hematíes, van a estar más cansados. Si no tienen eh plaquetas van a estar van a están más a riesgo a tener sangrados y si no tienen leucocitos, están más a riesgo de tener infecciones. ¿Cuál es la incidencia del síndrome melodisplásico? Pues mira, de esto en España teníamos muy pocos datos hasta ahora, pero han salido datos.
(09:33) es una es una enfermedad que es poco frecuente, o sea, es una no es una una enfermedad muy frecuente, pero eh bueno, es tiene un no esñable. Se espera que en 2025 se diagnostiquen 1730 personas en España con sírome melodisplásico. Eso hace que haya que la incidencia anual sea entre 3,929 casos por 100,000 habitantes año.
(09:58) Ya veis que no es una cosa que sea espectacularmente frecuente. Y los datos que han publicado este año parece que ha disminuido un poco, ¿no?, la incidencia anual entre 2009 y 2018, aunque esto es una estimación porque realmente hay probablemente 2020 en 2009 no se estudiaban a todos los pacientes como estud estudiamos probablemente ahora.
(10:20) Lo que es importante saber porque luego ya vais a ver que va a tener un peso muy grande en el momento del tratamiento, es que generalmente afectan a personas de edad avanzada, aproximadamente 75 años, ¿vale? Eh, y hay algunos factores de riesgo que son conocidos, ¿no? Como por ejemplo haber tenido un antecedente de otro cáncer, ¿no? Y haber recibido quimio y radioterapia previa.
(10:44) Eso puede aumentar el riesgo de tener un un síndrome mielodisplásico, estar expuesto a tóxicos. Esto aparece en todos los tumores y os lo han contado mucha gente, ¿no? Al benceno, ¿no? Estas cosas que tampoco estamos eh muy así la población general expuestos, pero que hay que preguntar, ¿no? E a productos químicos, ¿no? Por ejemplo, en la agricultura se utilizan mucho y hay que hay que preguntarlo.
(11:10) Y también hay algunos datos de que el tabaco aumenta el riesgo de síndrome de tener un síndrome melodisplásico, pero os tengo que decir que el impacto que tiene el tabaco en el síndrome melodisplásico está a años luz del impacto que tiene el tabaco en otras neoplasias como puede ser el tumor e los el cáncer de pulmón, pero sí que se asocia a un riesgo un poquito mayor de tener un síndrome melodisplásico.
(11:33) ¿Vale? Ya tenemos un paciente que se nos ha presentado con unas con unas células sanguíneas bajitas, ¿no? Con esa anemia, esa leucopenia y esa y esa o esa trombopenia. Y lo que vamos a tener que hacer es un diagnóstico, ¿no? Tenemos una sospecha y tenemos que diagnosticar. A día de hoy es imprescindible en el síndrome melodisplásico por múltiples cosas hacer lo que llamamos un diagnóstico integrado.
(11:58) Esto que significa que vamos a necesitar distintos especialistas que evalúen esa médula ósea. Serán los hematólogos, ¿no?, que harán esa morfología, los patólogos, ¿no?, que a veces eh hacemos un también una un una biopsia de médula ósea, una biopsia de ese hueso, será también eh los citogenetistas y no la gente de molecular, ¿no?, que que evalúen esta médula ósea en eh al completo y serán todos ellos los que darán un diagnóstico muy detallado de qué tipo de mielodisplásico eh tenemos, ¿no? Entonces, en morfología, ¿qué es
(12:36) esto de la morfología? Esto es esto es el campo de los hematólogos. Yo no soy fitóloga, pero es un el punto clave eh dentro de de síndrome mielodisplásico. Esto de mielodisplasia. Displasia significa células aberrantes que son de formas raras básicamente. Entonces para demostrar mirodisplasia, entre otras cosas, hay que mirar a ver si ese paciente tiene esas células con formas que llamamos raras, ¿no? Esa médula ósea con células que son extrañas o diferentes a lo normal.
(13:07) Esto es probablemente lo más complejo de todo el de todo el diagnóstico y aquí y se puede ver a veces en sangre periférica y en médula ósea, pero hay que es obligatorio para el diagnóstico del mielo disisplásico hacer la médula ósea. Aquí veis esto es una sangre periférica y esto es un una foto de una médula ósea.
(13:28) Pero el morfólogo o el citólogo o que generalmente es un hematólogo, tiene que contar cuánta displasia hay y contar también el porcentaje de blastos. ¿Y qué es esto? El de porcentaje de blastos. Bueno, pues los blastos son células inmaduras, ¿vale? Entonces, ya os he dicho que el problema en esta enfermedad es que las células mueren muy pronto.
(13:50) Entonces, a veces se acumulan en ese estadio de eh de blasto. Blastos tenemos todos, los normales también, pero los pacientes sanos, o sea, los sanos, yo todos tenemos blastos, pero en el mielodisplásico a veces están un poquito aumentados en número y hay que contar cuántos blastos tienes. Este es un punto muy importante porque además es lo que nos separa de una enfermedad un poquito más eh más agresiva que es la leucemia mieloblástica aguda.
(14:19) Y hay un punto de corte que es el 20% de blastos que que no que divide mielodisplasia versus mieloblástica aguda. Los síndromes mielodisplásicos ya vais a ver que no es obligatorio tener blastos, pero los pueden tener. Entonces, hay que contar. Por otro lado, tenemos eh la anatomía patológica. la anatomía patológica, los patólogos lo que hacen en España es eh porque en otros países no también ven esa parte de la morfología, pero en España ven el trozo de todo eso, igual que cualquier otro tejido, hacen sustinciones y caracterizan lo mismo que
(14:54) hacemos la morfología, que es en el líquido, ellos hacen en el hueso, ¿no?, el porcentaje de blastos, la displasia y además ven si hay o no fibrosis en la médula ósea, que también es un punto que tiene un que puede tener un impacto en el pronóstico y por eso a día de hoy es no os voy a decir obligado, pero es muy habitual hacer una biopsia ósea al diagnóstico.
(15:21) probablemente más allá del diagnóstico ya no tiene mucho impacto, pero muchos centros estamos haciendo el diagnóstico porque puede tener eh un un punto en el pronóstico y lo que es clave, ¿no?, es toda la parte de genética de en los milodisplásicos y es clave porque nos ayuda mucho a al diagnóstico y además tiene un impacto brutal en el pronóstico.
(15:48) en los mielobis clásicos es obligado a hacer un cariotipo. Ahí os pongo una foto de de que es un cariotipo. ¿Qué es un cariotipo? Pues cada cosita que veis aquí es un cromosoma y algunos pacientes les falta, ¿no?, eh, en el síndrome milisplásico, por ejemplo, aquí pues nosotros tenemos dos cromosomas, ¿no? De cada de cada número y por ejemplo aquí no hay tres cromosomas cuatro, tres cromosomas cinco, eso es una alteración, tres cromosomas 18, ¿no? O sea, quiero decir que mirar, estudiar los cromosomas tiene un impacto brutal para el pronóstico de
(16:22) estos pacientes y es obligatorio. Y lo que ha venido en los últimos años, que a veces nos cuesta más en tiempo porque esto el cariotipo en una semana generalmente lo tienes de vuelta, es el tema molecular, que es estudiar las mutaciones. Desde hace unos años, no pocos, 2017, pero ahora eh hace un par de años salió un índice pronóstico que los las incluye.
(16:48) Es vital hacer un estudio molecular de los pacientes con síndrome melodisplásico porque nos va a ayudar a separar los pacientes que tienen un riesgo mayor o los que tienen un riesgo menor, que de lo que vamos a hablar a continuación. Entonces, es muy importante hacer eh eh molecular al diagnóstico. A día de hoy en España se hacen en casi todos los centros y si no luego se hablaré un poco del grupo español de mielodisplasia.
(17:14) Hay opciones de que lo haga el grupo español de melodisplasia, pero eh es imprescindible para estimar el pronóstico de los pacientes con síndromes melodisplásicos. Y después de todo esto, ¿no? De tener al morfólogo mirando el el aspirado de médula ósea, ¿no? Eh, cómo son esas células, si tienen displasia o no. Mirar el eh el patólogo, ¿no? Eh, mirando si tiene fibrosis, si tiene blastos, si no tiene blastos, el genetista, ¿cómo están los cromosomas? si le falta algo, si no y demás y los la molecular, hay que hacer ese diagnóstico integrado porque
(17:48) el diagnóstico del mielodisplásico requiere siempre tener unas células bajas en en en el hemograma, ¿no? O anemia o trombopenia o neutropenia. y una de estos tres pilares, displasia, que son eran esas formas aberrantes, un porcentaje de blastos entre 5 y 19 o una clonalidad por cariotipo típica del mielodisplásico.
(18:13) Entonces, con citopenias y una de estas puedes tener más, pero con una de estas ya te valdría para hacer un diagnóstico de síndrome melodisplásico. Por eso los diagnósticos de síndrome mirodis clásico son difíciles y llevan tiempo porque a veces el tener todas estas pruebas de vuelta lleva puede llevar entre 15 días, 3 semanas, un mes.
(18:37) Entonces, a veces no es fácil eh tener un diagnóstico rápido porque además es imprescindible tener todas las pruebas de vueltas para hacer un un diagnóstico certero. Una vez que tenemos el diagnóstico, lo siguiente que hacemos con con eso es establecer el pronóstico. ¿Por qué? porque eso ya vais a ver que eh determina el tratamiento que vamos a poner.
(19:03) Entonces, es también lo mismo que el diagnóstico. Es tan importante el diagnóstico como el pronóstico. Y ya vais a ver que las características pronósticas, que os las voy a enseñar ahora mismo, eh algunas de ellas, bueno, ya las tenemos con porque las necesitamos a veces también para el diagnóstico. Entonces, ¿qué implica eh pronóstico, no? ¿Qué tiene peso en el pronóstico de los pacientes? pues el número y la intensidad de citopenias, ¿no? Citopenias es células bajas, luego el número y la profundidad de esa anemia, leucopenia o trombopenia. Es
(19:34) decir, si tú tienes anemia y leucopenia, es peor que tener anemia solo, ¿no? Entonces, número y profundidad. Eso es lo primero que tiene impacto en el pronóstico. Tiene impacto también el recuento de blastos, ¿no? Esas células inmaduras que os he dicho, ¿no? Que eh más de 20% se considera leucemia meloblástica aguda.
(19:57) Entre 5 y 19% entran a día de hoy en eh síndrome en clasificados como síndromes melodisplásicos en la gran mayoría de ellos. Entonces, eh tener más blastos, ¿no? Te pareces más a un a una leucemia aguda, pues es un poquito peor. Pero hayodis plásicos, insisto, que no tienen blastos, pero si tienes entre 5 y 19% de blastos, pues también es un punto malo en en cuanto al pronóstico.
(20:24) Y lo que más peso probablemente tiene en el pronóstico es las alteraciones en los cromosomas. Esto se ha complicado mucho porque teníamos un primer índice que tenía tres categorías. es el segundo eh un poco más moderno, ¿no? Tiene cinco categorías de citogenética de estas alteraciones del de los cromosomas, ¿no? Parece que vamos complicando esto, ¿no? Cada vez más, pero hay algunas alteraciones que son de peor pronóstico y por eso es tan importante tener un cariotipo al diagnóstico, ¿no? Ver esos cromosomas cómo son, si son normales, si
(20:56) tiene alguno de extra, si le falta alguno, ese tipo de cosas. Y lo que hemos añadido en los últimos años son esas mutaciones, esas alteraciones moleculares que también a día de hoy forman parte de el pronóstico. Y me vais a preguntar, «Pronóstico, pero pronóstico de qué, ¿no?» Bueno, pues esto hace una estimación del riesgo que tiene ese mielobis clásico de transformarse a una leucemia aguda, que ya hemos dicho que es una enfermedad un poquito más agresiva, más rápida, más rápida y el impacto que va a tener en la
(21:27) supervivencia de los pacientes. Entonces, con estos de características, en función del índice pronóstico, hacemos unos subgrupos de pacientes, ¿no? Que los dividimos, digo en función porque esto también cada vez hay más categorías, pero los dividimos en varios, ¿no? Riesgo, igual habéis oído, bajo, intermedio uno, intermedio dos o moderado, alto porque cambia dependiendo del índice pronóstico, pero lo que hacemos nosotros es dividirlos en dos.
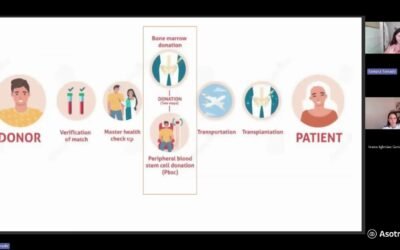
(21:55) salomónicamente, pacientes que tienen que son de bajo riesgo y pacientes que son de alto riesgo a la derecha. Esto es una Y, ¿por qué es importante? Porque e hay dos premisas en el e en el síndrome hemelodis plásico. Es una enfermedad de por vida, es una enfermedad que va a durarte siempre y la única manera de curar a estos pacientes es hacer un trasplante.
(22:19) Por eso, como es la única manera es es de curar a estos pacientes hacer un trasplante de médula ósea de un donante sano, o sea, un trasplante de otro de otra de otro sistema inmune, los pacientes que no tienen ese acceso a ese a esa a ese donante sano, pues van a van a continuar con esta enfermedad eh de por vida.
(22:40) Y además es importante porque es una enfermedad que es bastante heterogénea. Es decir, decir síndrome melodisplásico en 2025 no significa nada porque hay pacientes que tienen una supervivencia que se que puede ser muy similar a la de la población general y otros pacientes que tienen una supervivencia que se asemeja más a la de la leucemia aguda.
(23:02) Por eso es tan importante establecer el pronóstico de estos pacientes y ver si entran en esas características de alto o bajo riesgo. Vamos a empezar por el síndrome melodisplásico de bajo riesgo. Generalmente son pacientes que cursan habitualmente solo con anemia. Pueden tener otras cosas, pero suele ser habitualmente solo con anemia porque la anemia está presente en el 80% de los pacientes con mielobisplasia.
(23:27) Generalmente tiene pocos blastos, generalmente tiene un cariotipo esos cromosomas normales y son pacientes que tienen una supervivencia larga de años y que se transforman es más difícilmente en una leucemia aguda. Como objetivo general del tratamiento, nosotros en estos pacientes lo que hacemos es mejorar la calidad de vida y luego os voy a explicar por qué.
(23:51) Los pacientes de alto riesgo, sin embargo, pueden tener ahí se me ha colado, me falta una a anemia, leucopenia y trombopenia. A veces tienen las tres, pueden tener blastos, ¿no? Porque eso te da puntos para irte a ese lado del bajo del alto riesgo. A veces tienen esos cromosomas muy alterados y tiene una supervivencia, como os decía, peor que puede ser de meses y tiene una alta transformación a leucemia.
(24:15) Y el objetivo del tratamiento inicial es mejorar esa supervivencia, intentar evitar esa transformación de la leucemia, ¿no? Y mejorar esa supervivencia. Y esto lo vais a entender eh ahora, ¿no? Porque el problema, el uno de los problemas que tenemos en los síndromes melodisplásicos es que por desgracia, aunque hay muchísima investigación y hay muchísima y vienen probablemente muchos fármacos que pueden mejorar, la disponibilidad de los tratamientos no es mucha.
(24:44) Entonces separamos, hay que hacer, no hay que dejar el tratamiento para cuando realmente no va a hacer un cambio, va a tener un impacto en esa supervivencia de los pacientes. Entonces, como os decía, el paciente de bajo riesgo lo que hacemos es intentar mejorar su calidad de vida porque tiene poco riesgo de transformarse, poco riesgo de eh tener un impacto en la supervivencia.
(25:06) Entonces, en los pacientes que eh que tienen que solos que no tienen que no tienen una anemia que sea muy muy importante, pues se hace un tratamiento sintomático, solo se vigila de vez en cuando con análisis y vemos cómo va, ¿no? Cuando ya aparece la anemia, ¿no? Eh, y cuando la anemia ya empieza a tener un poquito de entidad, lo que hacemos es dar un soporte, ¿no? Intentar empujar a esa médula ósea, ¿no? para que produzca más más células.
(25:36) ¿Como con qué? Pues por ejemplo, para que produzca más glóbulos rojos con eritropolyetina. Básicamente lo que hacían los ciclistas hace unos años, ¿no? Si la si los glóbulos rojos eh son los son los responsables de transportar el oxígeno, ¿no? Pues si yo pongo más glóbulos rojos, pues más transporte de oxígeno hay.
(25:56) Entonces ellos se pinchaban esa eritropoyetina que lo hacían de manera ilegal. Pero nosotros no, este es un tratamiento que sirve para a los pacientes con anemia para subir esa población de globulos rojos, ¿no? Y para que tengan menos anemia durante un tiempo. Con la leucopenia nos pasa lo mismo. Tenemos otra especie de eritropoyetina que se llama GCSF, que también estimula a la médula producir eh leucocitos.
(26:21) Y en para la tromboplia existen los análogos de la trombopoyetina que se utilizan menos porque no están aprobados en el melodisplásico y porque generalmente cuando hay trombopenias muy profundas y suele haber alguna característica extra de alto riesgo y se suelen tratar como pacientes de alto riesgo. Si la anemia eh fracasa al tratamiento con eritropoyetina o no responder a laopilletina, el pilar extra, ¿no? de de del tratamiento de los síndromes mielodisplásicos.
(26:51) El gran pilar son las transfusiones, siempre están disponibles. Esto entre comillas tenemos, o sea, vivimos en una sociedad que es, o sea, que tiene una suerte tremenda porque tenemos muchísimos donantes de sangre, ¿no? Y que que están dando vida todos los días a estos pacientes con mielodisplasia. Hay otros otros países que no están en la misma situación.
(27:13) Así que desde aquí animo a todo el mundo a ser donante de sangre, pero eh a veces no mejora la calidad de vida porque tú le estás poniendo, ¿no?, esas glóbulos rojos que le faltan al paciente, pero es verdad que pueden tener otros efectos eh adversos como puede ser la sobrecarga de hierro. O sea, cuando uno pone mucha sangre extra, eh al final eh hay muchos eh hematíes ahí que se han roto y hay un exceso de hierro, ¿no?, que se puede depositar y que hay que controlar un poquito en estos pacientes con síndrome mirodisplásico. Esto no es las única la
(27:45) única opción. Hay algunos pacientes concretos que tienen tratamientos un poquito dirigidos, ¿no? Como puede ser la alenalidomida. La la lenalidomida son unas pastillas eh que eh ayudan mucho a mejorar la anemia eh en pacientes muy concretos, ¿no? En unos pacientes con un síndrome melodis plásico que se llama 5Q.
(28:08) Y eh también puede funcionar en el resto de pacientes con síndrome melodisplásico de bajo riesgo, pero responden muy muy poquitos de ellos. Por eso solo está aprobado en España para esos pacientes con 5q. es una opción en aquellos pacientes con cinco cumenos en los que o bien no responden a aritropoyetina o bien eh no son candidatos a la misma.
(28:28) Y lo de la misma manera tenemos otro fármaco que es se que tiene un nombre muy raro que se llama luz patercep y que se pone intravenoso y cada tr semanas y que es también eh muy eh muy bueno para el tratamiento de eh la anemia en pacientes con otro tipo de melodisplásico concreto que son los hideroblastos en anillo. ¿Vale? Entonces, hay opciones más allá de la eritropoyetina.
(28:55) Sí, a día de hoy en España tenemos estas estos dos fármacos para pacientes concretos y por eso ese diagnó proceso diagnóstico, ¿no?, y poner todas esas características con todos los puntos que os he dicho es tan importante porque luego puedes acceder a ciertos tratamientos. Este es el esquema que tenemos en el grupo español de melodisplasia ahora para el tratamiento de los síndromes melodisplásicos, que esto no es no es que sea, o sea, que no necesitéis eh conocerlo a fondo porque deberíamos conocerlo nosotros, pero que incluye
(29:25) todas esas eh todas esas opciones. Paciente que tiene una anemia, pero que es asintomática, seguir y si hay cambios eh volver a a reevaluar y en los pacientes que son sintomáticos, ¿no? que tiene una anemia ya un poquito más profunda con menos de 10 g, pues se puede utilizar la eritropolyetina en casos de con 5 menos la alenalidomida después de la eritropoyetina y en aquellos pacientes que no responden eh aritropoietina, que dejan de responder a aritropoietina y tienen esos hidroblastos en anillo, pues se puede
(29:58) utilizar el luz paterc. ¿Qué ocurre en el paciente de alto riesgo? ¿no? Pues en el paciente de alto riesgo eh es el paciente fetén para el tratamiento curativo, el trasplante halogénico. ¿Y por qué? Porque el trasplante halogénico es un tratamiento que no está exento de complicaciones. Tiene una una morbimortalidad, que eso significa que hay pacientes que tienen complicaciones del trasplante y que pueden morir por el trasplante alogénico, que no es desdeñable.
(30:31) Y por eso hay que hacer siempre esa balanza riesgo beneficio de trasplantar o no trasplantar a los pacientes. El objetivo del trasplante halogénico es eliminar esa hematopoyesis del paciente que está enferma y ponerle una hematopoyesis de un donante que sea sana. Generalmente eh se suele hacer o bien de un hermano, se puede hacer de un donante del registro de que est que eso también es un es un punto que que yo creo que es que tiene mucho eh mucha importancia y que hay que destacar.
(31:07) E en Europa hay un montón de donantes en el registro, o sea, hay como en el registro mundial hay como 40 millones y los la población europea está muy representada. Eso hace que casi todo el mundo vaya a encontrar a un donante en el registro. Y si no tiene hermanos, no, yo no tengo hermanos, luego eh si me ocurre, yo tendría que ir a un registro.
(31:27) Y la tercera fuente e pueden ser los hijos o los padres si no son muy mayores, son un tipo de donante un poquito distinto que es aploidéntico. Así que casi todo el mundo en nuestro medio que necesita un trasplante eh lo tiene. El problema que tiene el trasplante es que está muy eh que esa comorbilidad, ¿no? ese riesgo de tener una complicación grave, ese riesgo de fallecer, va también muy asociado, no tanto a la edad, porque a mí no me gusta decir a la edad, pero a la situación física de de del paciente. Entonces,
(31:58) para hacer un trasplante hay que hacer una evaluación muy completa del paciente como tal. Generalmente eh se dice que el trasplante son candidatos a trasplante aproximadamente a los hasta los 70 años. Ahora hay un margen, ¿no? Hasta los 75, si la población está muy bien, si el paciente está muy bien, pero el eh hay que hacer una evaluación muy completa a poder ser, ¿no?, pues con un geriatra detrás, ¿no?, que te ayude a a a calcular bien el riesgo que tiene de llevar a ese paciente a al trasplante.
(32:32) Y esto hace que esta opción curativa, ¿no?, No, el trasplante alogénico tan deseado, ¿no? Objetivo del paciente de alto riesgo. Como os he dicho que la mayoría de pacientes, la mediana de edad al diagnóstico 75 años, la mayoría de pacientes con síndrome de melodisplásicos no son candidatos a trasplante porque son una población mayor que ya tiene otras otras enfermedades, ¿no?, que le impide eh o sea, que hace que el trasplante alogénico sea una opción muy arriesgada, ¿no? y que no se haga porque el riesgo de fallecer del trasplante es mayor que
(33:07) el de que el de fallecer por la enfermedad. Así que generalmente se hace trasplante alogénico, ¿no? Como pone esas eh esa esta diapositiva a hasta los 70 años, yo diría 70 75 en función del paciente como está. O sea, ahora ya no hay un punto de corte como que que sea de la edad, eh, pero es verdad que entre los 70 y 75 hay que hacer una buena evaluación, no tiene que tener enfermedades relevantes asociadas y eh a veces hay que rehacer un tratamiento antes de quimioterapia o hace acetitidina para intentar eliminar la
(33:42) enfermedad. es mejor ir en respuesta, pero esto todavía es una incógnita porque ya vais a ver que e los tratamientos que tenemos para esta enfermedad, ¿no?, o sea, pues tienen alguno algunos peros y esto hace, ¿no?, la edad que no tenga que el paciente no tenga que tener comorbilidades y demás, que solo es real aproximadamente en un 15% de los melodis plásicos, o sea, de todos los melodisplásicos que que diagnosticamos al final a trasplante pues llegan entre un 15 un 20%.
(34:13) Probablemente algo ahora sea un poquito mayor esta cifra porque la gente llega a los 75 años fenomenal y hay que hay y estamos han aparecido nuevas formas de hacer trasplante y eso hace que hayamos aumentado un poquito la la edad eh a la que trasplantamos a los pacientes, pero son muy poquitos pacientes los que se benefician de de los que al final no son los que se benefician, sino los que al final llevan a un llegan al trasplante halogénico.
(34:46) Si no podemos hacer un trasplante halogénico, la opción eh eh el el tratamiento que tenemos a nuestra disposición es un tratamiento con un fármaco que se llama azacitidina, que es un fármaco que llamamos hipometilande. Este tratamiento lo que hace es una manera, ¿no? Como pone ahí en la diapositiva, educa la a la enfermedad a portarse bien.
(35:05) Es es decir, mejora, intenta mejorar esas anemias, ¿no? y la o esa anemia, esa trombopenia reduce el número de blastos, lo que ha lo que retrasa esa progresión a la leucemia y ha demostrado, ¿no?, que mejora la supervivencia de los pacientes con síndrome con síndromeisplásico. No hay límite de edad para recibirla, pero sí que hay algunos condicionantes.
(35:27) Esto se pone de manera subcutánea, ¿no? 7 días al mes. Habitualmente se hace de lunes a viernes, sábado y domingo descanso y luego otra vez lunes y martes. Y se repite, ¿no? cada 4 semanas desde el primer día. O sea, que al final esto implica que hay que ir 7 días al mes al hospital o tener a disposición eh un la eh la administración domiciliaria, que en España ahora hay muchas comunidades donde se puede poner eh a domicilio, pero no es en todas y eso hay que saberlo bien.
(35:57) Por lo tanto, es importante, además es un tratamiento que inicialmente puede aumentar un poquito más los requerimientos de de transfusiones porque al final no es tan selectivo de la célula madre mala. Entonces, no, al principio hay una competencia y mat mata lo bueno y lo malo y luego gana, debería ganar la partida, la parte buena, ¿no? Y recuperar la anemia, por lo que es importante que tenga apoyo familiar, que esté en unas condiciones buenas para ir al hospital y que tenga un buen acceso al hospital para el tratamiento y las
(36:26) complicaciones. Como os digo, se es el tratamiento generalmente es ambulatorio, se pone en hospital de día o en domicilio en algunos sitios. Son siete días al mes de manera subcutánea y eh hay que evaluar, sería bueno evaluar la enfermedad. A veces tarda un poquito en hacer respuesta, entonces hay que esperar cuatro o seis ciclos y si funciona hay que ponerlo de manera indefinida porque sabemos que si paramos la enfermedad va a volver, así que hay que ponerlo mientras funcione, ¿vale? y tiene algunos efectos adversos como que
(36:58) como os como os he dicho, ¿no? Al principio a veces se requiere más transfusiones porque destruye la médula ósea de manera temporal y ah puede producir alguna inflamación y algunas molestias en la zona de punción eh subcutánea. Los retos, pues hay que mejorar la respuesta porque este es el problema, ¿no? Eh algún el problema de la facitidina es que solo responden aproximadamente la mitad de pacientes.
(37:20) Luego esto es muy mejorable, ¿vale? que además hay que mejorar la duración de de la respuesta porque sabemos que todos los pacientes va a haber un momento que van que van a dejar de responder y además eh hay que intentar buscar opciones más allá de la zacitina porque cuando uno se hace refractoria la zacitina ya la supervivencia empieza a tambalear y es por eso que se deja la zacitidina solo para el paciente de alto riesgo para intentar utilizarlo realmente cuando el paciente se vaya a beneficiar, ¿no?, o esté a riesgo de esa
(37:52) transformación, ¿no? Entonces, se intenta sacar eh más partido a a este tratamiento. Evidente, ensayos clínicos con nuevos fármacos en eh si hay que ir a a un ensayo clínico porque todo esto dice, ¿no?, que este tratamiento es insuficiente y deberíamos buscar otras alternativas. Se puede utilizar la quimioterapia, sí, pero solo e es una es un tratamiento a dosis altas y es muy tóxico.
(38:19) Entonces, se utiliza únicamente en algunos casos en pacientes que se va a ir a que se va a ir a trasplante. Eh, no es una opción definitiva. Si la dejas vuelve a aparecer la enfermedad, por lo tanto, a veces se utiliza para reducir esa enfermedad antes del trasplante, pero tampoco en todos los casos, como os he dicho.
(38:38) Y este es el esquema de tratamiento en el grupo español de mielodisplasia. ¿Y qué es esto del grupo español de mielodisplasia? Ya estoy terminando. Es un grupo de investigación nacional que funciona muy bien, que incluye 140 centros españoles, que seguro que la mayoría de vuestros centros, porque ahí están la mayoría de los centros, están incluidos dentro de este grupo.
(38:58) Hay centros grandes, centros pequeños, centros de todo tipo. incluye más de 400 investigadores, no solo médicos, hay genetistas, hay biólogos, hay muchísima tipo de gente que participa en este grupo y que el fin es mejorar el conocimiento de la enfermedad y mejorar el tratamiento, pronóstico y cuidados de los pacientes. Tiene un registro en el que participan más de 16,000 pacientes y hacemos guías clínicas.
(39:24) Hemos hecho unas en 2012, unas en 2020, las de 2024 están a punto de eh de salir y hemos hecho, hicimos una guía para pacientes, que os he dich he dejado ahí el QR por si lo queréis descargar, donde está explicado la enfermedad muy bien, cuando cómo son cómo se diagnostica, cuáles son los síntomas eh que pueden aparecer, cómo le cómo la tratamos.
(39:47) Y tenemos además un área en el en la página web un área de ensayos clínicos dentre donde cada uno de los investigadores pone los ensayos clínicos a disposición del resto por si alguno quiere mandar a otro centro eh pacientes para que se para que disfruten de estos ensayos clínicos. Y tenemos también un área de pacientes que está coordinada por la doctora Hernández de Granada y que hace una reunión anual eh de pacientes que es muy interesante en la que aprendemos todos porque eh eh esto es una enfermedad que ya veis que es compleja para vosotros, también para
(40:19) nosotros y nosotros necesitamos saber qué es lo que queréis vosotros los pacientes. Ahí os dejo la página web de del grupo y con esto ya termino con las conclusiones. Primero, no estáis solos, es poco frecuente, pero existen muchos médicos con gran experiencia y hay tratamientos y asociaciones de pacientes que os pueden acompañar.
(40:39) El diagnóstico ha mejorado mucho en en los últimos años y ahora con las técnicas, ¿no?, de genética avanzada somos capaces de predecir muy bien lo que va a ocurrir y hacer unos tratamientos muchísimo más personalizados. Hay tratamientos que son eficaces, que mejoran los síntomas, la calidad de vida y la supervivencia. La investigación está avanzando mucho gracias a algunos eh ensayos clínicos, a grupos de trabajo.
(41:06) Cada vez eh tenemos terapias más eficaces y menos agresivas. El seguimiento y el cuidado constante son son clave, o sea, hay que estar muy controlado, mantener una conversación fluida como un elematólogo. Hay que hablar de lo que quieres, de lo que no quieres, de lo que necesitas, de lo que te pasa con tu con el con el hematólogo.
(41:24) Y yo siempre te acabo diciendo que la actitud importa, siempre eh importa. Es normal tener miedo o dudas, eh, pero eh preguntar en la consulta, porque muchas veces eh el miedo viene por el desconocimiento. Nadie os va a poder una dar una hoja de ruta en una enfermedadológica. nadie va a poder eh poneros fechas a a a lo que va a ocurrir, pero sí que os puede dar un poco un una visión de qué puede ocurrir y cómo va a ocurrir.
(41:53) Y yo creo que importante es muy importante eh preguntar y mantener desde luego una actitud positiva porque hay muchas razones, esto está cambiando mucho y hay muchas razones para tener esperanza en los síndromes modisplásicos. Y con esto ya termino. Muchas gracias. Muchísimas gracias por la ponencia, gracias por ayudarnos a entender qué es esto de los síndromes mirodis plásicos y también creo que es de agradecernos el poder hacerlo de una manera tan accesible a la población general, pues suerdo a los que no tenemos conocimiento
(42:32) sobre esta enfermedad, ¿no? Así que eh bueno, desde Asotrame eh queremos agradecerte muchísimo. Gracias a vosotros esta ponencia. Así que nada, un abrazo a todos los que nos estáis viendo y y os esperamos en futuros encuentros.